题目内容
14.早在春秋战国时期,我国就开始生产和使用铁器.写出以赤铁矿(主要成分Fe2O3)为原料炼铁的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.分析 工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,写出反应的化学方程式即可.
解答 解:工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
点评 本题难度不大,掌握工业上炼铁的反应原理、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
4.下列叙述中不正确的是( )
| A. | 钠原子失去电子后变成钠离子 | B. | 氯离子失去电子变成氯原子 | ||
| C. | 化学变化中分子不能再分 | D. | 原子的质量主要集中在原子核上 |
5.下列有关水的说法不正确的是( )
| A. | 水是生命活动中不可缺少的物质 | |
| B. | 水通电分解和水的蒸发都是化学变化 | |
| C. | 用肥皂水可以检验硬水和软水 | |
| D. | 净化水的方法有吸附、沉淀、过滤和蒸馏等 |
2.在我们的日常生活中无时无刻不在发生着变化,下列变化过程中不包含化学变化的是( )
| A. | 阳台上的铁制栏杆在梅雨季节生锈了 | |
| B. | 广州亚运会开幕式上,舞台工作人员用干冰制造“云雾” | |
| C. | 将米饭或馒头放入口中咀嚼一会儿后感到有甜味 | |
| D. | 上诲世博会开幕式上,漫天的烟花竞相绽放、精彩纷呈 |
3.某中学化学兴趣小组通过实验测定某大理石中碳酸钙的质量分数,将盛有20.0g该样品的烧杯放在电子秤上,倒入100.0g稀盐酸(假设大理石样品中的杂质不与稀盐酸反应,也不溶于水),使该样品恰好完全反应,实验过程中的有关数据如下表所示:
计算:
(1)生成二氧化碳的质量.
(2)该大理石中碳酸钙的质量分数;
(3)反应完成所得溶液中溶质的质量分数(精确到0.1%)
| 时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
| 烧杯与所盛物质质量/g | 174.0 | 171.0 | 169.0 | 168.0 | 167.4 | 167.4 |
(1)生成二氧化碳的质量.
(2)该大理石中碳酸钙的质量分数;
(3)反应完成所得溶液中溶质的质量分数(精确到0.1%)
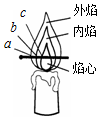 化学兴趣小组的同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.
化学兴趣小组的同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.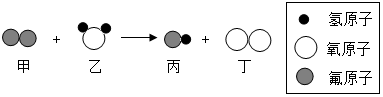
 为了研究炼铁原理,我市某校九年级综合实践活动小组按如图所示,用一氧化碳与氧化铁反应进行实验,现请你一起参与.
为了研究炼铁原理,我市某校九年级综合实践活动小组按如图所示,用一氧化碳与氧化铁反应进行实验,现请你一起参与.