题目内容
15.长期饮用硬水可能会引起体内结石,在生活中要将硬水软化可采用的方法是煮沸.分析 从硬水的成分和如何简单有效的消除硬水成分进行考虑.
解答 解:硬水是指含有较多钙、镁离子的水,煮沸能使钙、镁离子形成沉淀析出,这是生活中最常用的最简单的降低水硬度的方法.
故答案为:煮沸.
点评 该题能帮助学生了解化学在生活中的应用,体会学以致用的快乐.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.下列各项中,不属于模型的是( )
| A. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 红磷燃烧 | B. |  水分子 | ||
| C. | Na 金属钠元素 | D. |  一种原子结构 |
3.下列图示实验操作正确的是( )
| A. | 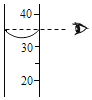 读液体体积 | B. | 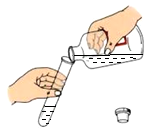 倾倒液体 | C. |  闻气体气味 | D. | 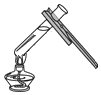 给液体加热 |
10.设计实验证明生石灰的确能与水发生反应.
(1)问题:通过有关实验证明生石灰能与水发生化学反应.
(2)资料收集:氧化钙能与水反应放出大量的热,氢氧化钙的水溶液能使酚酞试液变红
(3)提出猜测:氧化钙能与水反应生成氢氧化钙
(4)填写如表:
(1)问题:通过有关实验证明生石灰能与水发生化学反应.
(2)资料收集:氧化钙能与水反应放出大量的热,氢氧化钙的水溶液能使酚酞试液变红
(3)提出猜测:氧化钙能与水反应生成氢氧化钙
(4)填写如表:
| 实验步骤 | 观察到的现象 | 分析和结论 |
20.某同学用25℃的水溶解一定量的氯化钾,充分搅拌后发现杯底还有部分氯化钾固体没有溶解,然后该同学又用酒精灯加热至50℃,固体全部溶解.那么在加热前后,以下各量没有发生改变的是( )
| A. | 氯化钾的溶解度 | B. | 溶质的质量 | C. | 溶剂的质量 | D. | 溶质的质量分数 |
7.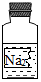 化学兴趣小组的同学发现实验台上有一瓶标签残缺的试剂(如图),同学们对此进行了如下探究.
化学兴趣小组的同学发现实验台上有一瓶标签残缺的试剂(如图),同学们对此进行了如下探究.
【提出问题】这是一瓶什么溶液?
【猜想与假设】海天同学的猜想是Na2SO3溶液;刘浩同学的猜想是Na2SO4溶液;你的猜想是Na2CO3(写一种).
【查阅资料】
Ⅰ白色沉淀BaSO3不溶于水,但要溶于稀盐酸.
Ⅱ硝酸具有强氧化性,能将BaSO3氧化成BaSO4.
ⅢNa2SO3与稀盐酸反应产生SO2,SO2能使石灰水变浑浊,也能使品红溶液褪色.
【进行实验】
Ⅰ海天同学取适量的该溶液于试管中,滴加稀盐酸,产生无色气体,他认为自己的猜想成立,而刘浩同学认为他的结论不合理,原因是与稀盐酸反应产生无色气体的并非只有Na2SO3.
Ⅱ刘浩同学为了验证自己的猜想,做了如下实验:
取适量的该溶液于试管中,先滴加足量的BaCl2溶液,再滴加过量稀硝酸,现象为先产生白色沉淀,加入稀硝酸沉淀不溶解,刘浩同学认为自己的猜想成立.
Ⅲ卓玛同学对刘浩同学的猜想又提出了质疑,她认为加BaCl2和稀硝酸,Na2SO3也会产生沉淀,为了验证自己的观点,做了如下实验:
写出卓玛同学实验过程中的化学方程式:Na2SO3+BaCl2=BaSO3↓+2NaCl,BaSO3+2HCl=BaCl2+H2O+SO2↑.
 化学兴趣小组的同学发现实验台上有一瓶标签残缺的试剂(如图),同学们对此进行了如下探究.
化学兴趣小组的同学发现实验台上有一瓶标签残缺的试剂(如图),同学们对此进行了如下探究.【提出问题】这是一瓶什么溶液?
【猜想与假设】海天同学的猜想是Na2SO3溶液;刘浩同学的猜想是Na2SO4溶液;你的猜想是Na2CO3(写一种).
【查阅资料】
Ⅰ白色沉淀BaSO3不溶于水,但要溶于稀盐酸.
Ⅱ硝酸具有强氧化性,能将BaSO3氧化成BaSO4.
ⅢNa2SO3与稀盐酸反应产生SO2,SO2能使石灰水变浑浊,也能使品红溶液褪色.
【进行实验】
Ⅰ海天同学取适量的该溶液于试管中,滴加稀盐酸,产生无色气体,他认为自己的猜想成立,而刘浩同学认为他的结论不合理,原因是与稀盐酸反应产生无色气体的并非只有Na2SO3.
Ⅱ刘浩同学为了验证自己的猜想,做了如下实验:
取适量的该溶液于试管中,先滴加足量的BaCl2溶液,再滴加过量稀硝酸,现象为先产生白色沉淀,加入稀硝酸沉淀不溶解,刘浩同学认为自己的猜想成立.
Ⅲ卓玛同学对刘浩同学的猜想又提出了质疑,她认为加BaCl2和稀硝酸,Na2SO3也会产生沉淀,为了验证自己的观点,做了如下实验:
| 步骤 | 操作 | 实验现象 | 实验结论 |
| 步骤1 | 取少量该溶液于试管中,滴加足量的BaCl2溶液 | 产生白色沉淀 | 无 |
| 步骤2 | 向步骤1的试管中滴加足量的稀盐酸 | 白色沉淀溶解,有气泡产生 | 此溶液不是Na2SO4 |
| 步骤3 | 将步骤2中产生的气体通入品红溶液 | 品红溶液褪色 | 此溶液是Na2SO3 |