题目内容
4.某物质X在氧气中燃烧的化学方程式为:2X+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O,下列说法正确的是CA.X中一定含有碳、氢元素,可能含有氧元素 B.X可能是氧化物
C.反应中生成物二氧化碳与水的质量比为88:72 D.X的相对分子质量为32.
分析 化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和;
化学反应前后,元素的种类不变,原子的种类、总个数不变.
解答 解:由2X+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O可知,反应后碳原子是2个,反应前应该是2个,包含在2X中;
反应后氧原子是8个,反应前应该是8个,其中2个包含在2X中;
反应后氢原子是8个,反应前应该是8个,包含在2X中;
由分析可知,每个X中含有1个碳原子、1个氧原子和4个氢原子,化学式是CH4O;
A、X中含有碳元素、氢元素和氧元素,该选项说法不正确;
B、X中含有三种元素,不属于氧化物,该选项说法不正确;
C、反应中生成物二氧化碳与水的质量比为:(44×2):(18×4)=88:72,该选项说法正确;
D、X的相对分子质量为:12+1×4+16=32.
故选:C.
故填:32.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
15.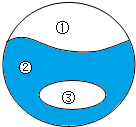 如图为物质的分类关系.①与②是并列关系,③包含在②中,若②是纯净物,则③不可能是( )
如图为物质的分类关系.①与②是并列关系,③包含在②中,若②是纯净物,则③不可能是( )
 如图为物质的分类关系.①与②是并列关系,③包含在②中,若②是纯净物,则③不可能是( )
如图为物质的分类关系.①与②是并列关系,③包含在②中,若②是纯净物,则③不可能是( )| A. | 二氧化碳 | B. | 高锰酸钾 | C. | 空气 | D. | 铜 |
19.谚语诗词中蕴含着科学道理.下列解释不正确的是( )
| A. | 真金不怕火炼-黄金化学性质不活泼 | |
| B. | 众人拾柴火焰高-可燃物越多,着火点越低,越容易着火 | |
| C. | 蜡烛成灰泪始干-泪是指石蜡液体 | |
| D. | 有麝自来香,不用大风扬-麝香的原因是分子在不停地运动 |
9.下列说法正确的是( )
| A. | 12g碳可以和16g氧气反应生成28g二氧化碳 | |
| B. | 12g碳可以和16g氧气反应生成28g一氧化碳 | |
| C. | 2g氢气和8g氧气反应生成10g水 | |
| D. | 2g氢气和16g氧气反应生成18g水 |
16.某同学用50mL的量筒取液体积时,仰视读数为20.0mL,则实际液体体积( )
| A. | 等于20.0mL | B. | 等于50mL | C. | 小于20.0mL | D. | 大于20.0mL |
13.小李同学编写的化学小报中有如下标题,其中标题下文章中的主角是一氧化碳,该标题可能是( )
| A. | PM2.5与雾霾天气 | B. | 新装修房屋内空气中的杀手 | ||
| C. | 形成酸雨的罪魁祸首 | D. | 燃气热水器安装在居室内的危险 |
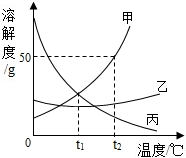 如图是甲、乙、丙三种固体物质的溶解度曲线,请回答:
如图是甲、乙、丙三种固体物质的溶解度曲线,请回答: