题目内容
8.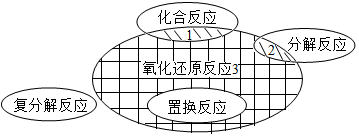 化学反应的基本类型有四种(化合、分解、置换和复分解反应),其中,化学反应前后有元素化合价发生改变的反应属于氧化还原反应,他们的关系如图所示.下列反应中只属于阴影“3”处的化学反应是( )
化学反应的基本类型有四种(化合、分解、置换和复分解反应),其中,化学反应前后有元素化合价发生改变的反应属于氧化还原反应,他们的关系如图所示.下列反应中只属于阴影“3”处的化学反应是( )| A. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | B. | 2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | ||
| C. | NaHCO3+HCl=NaCl+H2O+CO2↑ | D. | Fe+CuSO4=FeSO4+Cu |
分析 根据该反应中反应物、生成物的特点进行分析,阴影“3”处的化学反应是既不属于化合,又不是分解、置换.
解答 解:A.Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2反应中Fe2O3作为氧化剂;CO作为还原剂,该反应中的反应物是两种化合物,生成物是单质和化合物,不满足置换反应的定义,不属于置换反应,但是铁和碳的化合价都发生了改变,该反应属于氧化还原反应,符合;
B.2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,符合“一变多”的特点,属于分解反应,不符合;
C.NaHCO3+HCl═NaCl+H2O+CO2↑,没有元素化合价变化,不符合;
D.Fe+CuSO4 ═FeSO4+Cu,是置换反应,不符合;
答案:A.
点评 本题主要考查了化学反应的基本类型与物质中元素化合价的关系,解题的关键是根据各类反应中物质的种类及组成特点,分析化合价的变化.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
19.将质量分数为80%和20%的两种硫酸溶液混合后,所得溶液中溶质的质量分数不可能是( )
| A. | 19% | B. | 50% | C. | 60% | D. | 70% |
13.某班甲、乙两组同学分别做常见酸和碱与指示剂反应的实验,使用的试剂有稀盐酸、稀硫酸、氢氧化钠溶液和酚酞试液.实验后废液分别集中到各组的一个废液缸中.研究小组对两个组的废液进行检测,结果如下表.下列说法错误的是(不考虑酚酞和水)( )
| 废液来源 | 甲组 | 乙组 |
| 检测方法与结果 | 观察废液呈无色 | 观察废液呈红色 |
| A. | 甲组废液中可能含有稀盐酸和稀硫酸 | |
| B. | 乙组废液中一定含有氢氧化钠 | |
| C. | 直接将甲组的废液排入铸铁管下水道,可能腐蚀铸铁水管 | |
| D. | 乙组呈红色是因为氢氧化钠溶液遇到酚酞试液会变红色 |
18.相似性的背后往往是具备共同的特征,很多酸具有许多相似化学性质的原因是( )
| A. | 它们都是溶液 | B. | 它们都含有酸根离子 | ||
| C. | 它们都含有氢元素 | D. | 它们电离出的阳离子都是氢离子 |