题目内容
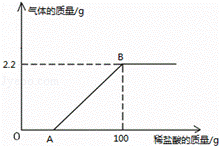
用100g含杂质3.2%的生铁粉(杂质不参与反应),与质量分数为10%的稀硫酸恰好完全反应制硫酸亚铁。求消耗的稀硫酸质量。
解:设消 耗稀硫酸的质量为x
耗稀硫酸的质量为x
Fe + H2SO4 = FeSO4 + H2↑ (1分)
56 98
100g×(1-3.2%) x×10%
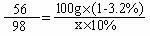 (1分)
(1分)
x = 1694g (1分)
答:消耗的稀硫酸质量为1694g。(设答正确1分)

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
下列物质间的转化,在一定条件下均能一步实现的是
| ①C→CO→CO2 | ②Cu→CuO→CuSO4 | ||
| ③Na2CO3→NaCl→NaNO3 | ④CaCO3→CaO→Ca(OH)2 | ||
| A.①②③ | B.①③④ | C.①②④ | D.①②③④ |
|
 (1)从微观角度看物质的变化是化学的思维方式之一。下面两幅示意图分别表示生成氯化钠的不同化学反应。请根据图示回答相关问题:
(1)从微观角度看物质的变化是化学的思维方式之一。下面两幅示意图分别表示生成氯化钠的不同化学反应。请根据图示回答相关问题:
|

|
|
|
| ||||||||||
| |||||||||||
| |||||||||||
 | |||||||||||
| |||||||||||
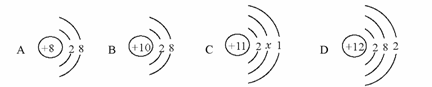
①图1是金属钠与氯气反应生成氯化钠的微观示意图。由图1可知,元素的化学性质与
其微粒的 (填字母序号)有密切关系。
A.最外层电子数 B.内层电子数 C.电子层数 D.核电荷数
②图2描述了NaOH溶液与盐酸反应的微观实质是 。
(2)用质量分数为6%的氯化钠溶液(密度为1.04g/cm3),配制100g质量分数为3%的
氯化钠溶液。配制过程为:
①计算(计算结果保留一位小数) :需6%的氯化钠溶液 mL(计算的依据
:需6%的氯化钠溶液 mL(计算的依据
是 ),水 g。
②量取;③ ;④装瓶、贴标签。