题目内容
用含80%的氧化铁的赤铁矿作原料,生产50t含4%杂质的生铁,理论上需多少吨赤铁矿?
考点:含杂质物质的化学反应的有关计算
专题:有关化学方程式的计算
分析:由生铁的质量、生铁中杂质的质量分数、赤铁矿石中氧化铁的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出需要含氧化铁80%的赤铁矿的质量.
解答:解:设需要含氧化铁80%的赤铁矿质量为x.
Fe2O3+3CO
2Fe+3CO2
160 112
80%x 50t×(1-4%)
=
x≈85.7t
答:需要含氧化铁80%的赤铁矿质量为85.7t.
Fe2O3+3CO
| ||
160 112
80%x 50t×(1-4%)
| 160 |
| 112 |
| 80%x |
| 50t×(1-4%) |
答:需要含氧化铁80%的赤铁矿质量为85.7t.
点评:本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.

练习册系列答案
相关题目
紫杉醇(分子式C47H51NO14)是从红豆杉科植物红豆杉的干燥根、枝叶以及树皮里面提炼出来的一种白色结晶体粉末,用于肺癌、大肠癌、头颈部癌、淋巴瘤、脑瘤的治疗.下列关于紫杉醇的认识错误的是( )
| A、紫杉醇里有47个碳原子 |
| B、紫杉醇是由分子组成的 |
| C、紫杉醇里碳元素的质量分数最大 |
| D、紫杉醇中碳、氢、氮、氧原子的个数比为47:51:1:14 |
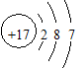 ,则它的电子数为
,则它的电子数为