题目内容
4.下列各组溶液,不加其它试剂就能鉴别的是( )| A. | NaOH、KCl、KNO3、FeCl3 | B. | Na2SO4、BaCl2、KNO3、NaCl | ||
| C. | K2SO4、Na2CO3、BaCl2、稀HNO3 | D. | Na2CO3、稀H2SO4、稀HCl、NaNO3 |
分析 在不另加试剂就能鉴别的题目中,首先观察有无有特殊颜色的物质,若有,将有颜色的溶液鉴别出来,然后再借用这种溶液鉴别其它溶液把其它没有确定出的物质确定出来;若都没有颜色就将溶液两两混合,根据混合后的现象进行分析鉴别.
解答 解:A、FeCl3溶液呈黄色,首先鉴别出黄色的FeCl3溶液;把FeCl3溶液与另外三种溶液混合,出现红褐色沉淀的溶液为NaOH溶液;但其余两两混合均没有明显现象,故不加其他试剂无法鉴别.
B、组内四种物质的溶液两两混合时,Na2SO4、BaCl2溶液反应能产生白色沉淀,但其余两两混合均没有明显现象,故不加其他试剂无法鉴别.
C、组内四种物质的溶液两两混合时,其中有一种溶液与其它三种溶液混合时出现一次白色沉淀和一次放出气体,该溶液为碳酸钠溶液;与碳酸钠溶液产生气体的溶液为稀HNO3,产生白色沉淀的为氯化钡;与碳酸钠溶液混合无任何明显现象的为K2SO4溶液;故不加其他试剂可以鉴别.
D、组内四种物质的溶液两两混合时,Na2CO3溶液与稀H2SO4、稀HCl反应均能产生无色气体,但其余两两混合均没有明显现象,故不加其他试剂无法鉴别.
故选:C.
点评 解答不另加试剂就能鉴别的题目时,若选项中有带色的离子,首先鉴别,然后再鉴别其它的物质;若都没有颜色,可将溶液两两混合,根据混合后的现象进行鉴别.

练习册系列答案
相关题目
14.根据初中化学酸、碱、盐的知识可知,将蓝色的硫酸铜溶液与氢氧化钠溶液混合后,可得到蓝色沉淀,其反应的化学方程式为CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
小军和小亮分别进行如下硫酸铜与氢氧化钠反应的性质实验探究:
(1)小军将上述有蓝色沉淀的浊液进行加热,发现沉淀变黑;
(2)小亮做这个实验时,在试管中倒入2mL CuSO4溶液,再加入一定量NaOH溶液,结果并没有得到蓝色的沉淀,而是浅绿色的沉淀;将此浊液加热直至沸腾,仍然观察不到有黑色的物质生成.
(思 考)①黑色物质是什么?②浅绿色的沉淀是什么?
(资料卡)
①氢氧化铜加热可以分解成2种氧化物;
②Cu4(OH)6SO4是一种浅绿色物质,溶解度极小,可溶于酸液;
③反应物的量不同,则生成物可能有所不同.
(3)通过查找资料卡得知:蓝色沉淀加热生成一种黑色物质的化学方程式为Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O,
浅绿色的沉淀是Cu4(OH)6SO4,其化学名称是碱式硫酸铜,生成该沉淀的化学方程式为:
4CuS04+6NaOH═Cu4(OH)6S04↓+3Na2SO4.
(实验探究)
(4)证明该浅绿色沉淀中含有S042-,他俩共同设计如下方案:
多次洗涤沉淀的目的是将沉淀表面附着的Na2SO4溶液洗净,防止其中的SO42-干扰实验,稀盐酸溶解浅绿色沉淀的化学方程式为Cu4(OH)6SO4+6HCl═CuSO4+3CuCl2+6H2O.
小军和小亮分别进行如下硫酸铜与氢氧化钠反应的性质实验探究:
(1)小军将上述有蓝色沉淀的浊液进行加热,发现沉淀变黑;
(2)小亮做这个实验时,在试管中倒入2mL CuSO4溶液,再加入一定量NaOH溶液,结果并没有得到蓝色的沉淀,而是浅绿色的沉淀;将此浊液加热直至沸腾,仍然观察不到有黑色的物质生成.
(思 考)①黑色物质是什么?②浅绿色的沉淀是什么?
(资料卡)
①氢氧化铜加热可以分解成2种氧化物;
②Cu4(OH)6SO4是一种浅绿色物质,溶解度极小,可溶于酸液;
③反应物的量不同,则生成物可能有所不同.
(3)通过查找资料卡得知:蓝色沉淀加热生成一种黑色物质的化学方程式为Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O,
浅绿色的沉淀是Cu4(OH)6SO4,其化学名称是碱式硫酸铜,生成该沉淀的化学方程式为:
4CuS04+6NaOH═Cu4(OH)6S04↓+3Na2SO4.
(实验探究)
(4)证明该浅绿色沉淀中含有S042-,他俩共同设计如下方案:
| 操作步骤 | 实验现象 | 结论 |
| ①将浅绿色的浊液过滤,并把得到的浅绿色沉淀用蒸馏水多次洗涤,直至取最后一次洗涤液,滴加BaCl2溶液. | 无现象 | 沉淀表面无Na2SO4残留(附着)或者已经洗净 |
| ②用稀盐酸溶解浅绿色沉淀,再滴加BaCl2溶液. | 有大量白色沉淀生成 | 沉淀中含有SO42- |
15.下列选用的除杂试剂和实验操作不正确的是( )
| 组别 | 物质 | 杂质 | 所选试剂(或操作) |
| A | HCl | H2SO4 | 加适量氯化钡溶液、过滤 |
| B | CaCl2 | CaCO3 | 加水溶解、过滤、蒸发 |
| C | Fe | Cu | 加过量稀盐酸、过滤 |
| D | CO | CO2 | 通入足量氢氧化钠溶液、干燥 |
| A. | A | B. | B | C. | C | D. | D |
19.下列有关原子的说法正确的是( )
| A. | 原子能构成分子,不能直接构成物质 | |
| B. | 碳-12原子和碳-13原子的中子数相同 | |
| C. | 原子在化学变化中不能再分,只能重新组合 | |
| D. | 原子中一定含有质子、中子、电子 |
9. 在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.该组同学对该实验进行了一系列的研究.
在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.该组同学对该实验进行了一系列的研究.
(1)溶液M的可能组成:
猜想①:是Ca(OH)2,
猜想②:是CaCl2(查资料知CaCl2水溶液呈中性).
为了确定其组成,同学们设计了如表方案并进行实验:
(2)若猜想①正确,则上述过滤后得到的澄清滤液中可能含有的溶质:
[提出假设]猜想一:NaOH和Na2CO3; 猜想二:Ca(OH)2和NaOH;猜想三:NaOH.
[设计实验]设计实验方案确定滤液中溶质的组成.
[反思拓展]在分析化学反应后所得物质的成分时,除了考虑生成物外,还需要考虑反应物是否过量.
 在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.该组同学对该实验进行了一系列的研究.
在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.该组同学对该实验进行了一系列的研究.(1)溶液M的可能组成:
猜想①:是Ca(OH)2,
猜想②:是CaCl2(查资料知CaCl2水溶液呈中性).
为了确定其组成,同学们设计了如表方案并进行实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于试管中,向其中滴加酚酞 | 溶液变成红色 | 猜想①正确 |
[提出假设]猜想一:NaOH和Na2CO3; 猜想二:Ca(OH)2和NaOH;猜想三:NaOH.
[设计实验]设计实验方案确定滤液中溶质的组成.
| 实验操作 | 实验现象 | 实验结论 |
| 分别取少量滤液于A、B两支试管中,A中加入CaCl2溶液,B中加入Na2CO3溶液溶液 | 若A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
| 若A中没有沉淀,B中产生沉淀 | “猜想二”成立 | |
| 若A.B中都没有沉淀 | “猜想三”成立 |
16.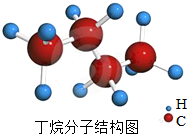 丁烷是重要的燃料和化工原料,日常生活中用打火机作燃料.下列有关叙述正确的是( )
丁烷是重要的燃料和化工原料,日常生活中用打火机作燃料.下列有关叙述正确的是( )
 丁烷是重要的燃料和化工原料,日常生活中用打火机作燃料.下列有关叙述正确的是( )
丁烷是重要的燃料和化工原料,日常生活中用打火机作燃料.下列有关叙述正确的是( )| A. | 丁烷由碳、氢元素构成 | B. | 每个丁烷分子中有14个原子 | ||
| C. | 此分子中电子总数等于中子总数 | D. | 次有机物中只含有两种原子 |
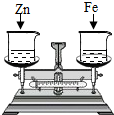 如图所示,烧杯中盛有质量相等、质量分数相等的稀盐酸,天平调平后,同时向其中分别加入等质量的锌片和铁片(形状影响忽略不计),则从反应开始到充分反应的过程中,天平指针指向的变化是B
如图所示,烧杯中盛有质量相等、质量分数相等的稀盐酸,天平调平后,同时向其中分别加入等质量的锌片和铁片(形状影响忽略不计),则从反应开始到充分反应的过程中,天平指针指向的变化是B