题目内容
18.某兴趣小组在实验室制取氧气,取来12.25克的氯酸钾和2克二氧化锰混合,加热一定时间后,冷却称量剩余固体质量为11.85克,请回答:(1)制得氧气质量为2.4克.
(2)将剩余固体溶解过滤得到的滤渣是二氧化锰(填物质的名称),质量为2克.
(3)生成的氯化钾的质量为多少克?
分析 反应前后的质量差即为反应生成氧气的质量,根据氧气的质量可以计算生成氯化钾的质量和氯酸钾的质量,进一步可以计算二氧化锰的质量.
解答 解:(1)生成氧气的质量为:12.25g+2g-11.85g=2.4g,故填:2.4;
(2)因为二氧化锰不溶于水,且反应前后质量不变,故将剩余固体溶解过滤得到的滤渣是二氧化锰,质量为2克.
(3)设反应生成氯化钾的质量为y,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,
149 96
x 2.4g
则$\frac{149}{96}=\frac{x}{2.4g}$,解得x=3.725g,
答:生成的氯化钾的质量为3.725g.
故答案为:
(1)2.4;(2)二氧化锰,2.(3)3.725.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
10.下列方程式书写正确的是( )
| A. | CO2+CaCl2+H2O═CaCO3↓+2HCl | B. | NH4HCO3+HCl═NH4Cl+CO2↑+H2O | ||
| C. | FeSO4+Cu═CuSO4+Fe | D. | Fe+2HNO3═Fe(NO3)2+H2↑ |
17.符号“2SO2”表示的意义是( )
| A. | 2个硫原子和4个氧原子 | B. | 2个二氧化硫分子 | ||
| C. | 2个硫原子和2个氧原子 | D. | 2个硫原子和2个氧分子 |
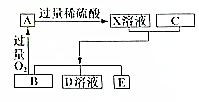 A、B、C、D、E均为初中化学常见的而物质,其中B、C均为金属,B为红色,它们的相对原子质量相差8,D溶液溶质只有一种,E为气体单质,如图是它们之间的相互转化关系,请回答:
A、B、C、D、E均为初中化学常见的而物质,其中B、C均为金属,B为红色,它们的相对原子质量相差8,D溶液溶质只有一种,E为气体单质,如图是它们之间的相互转化关系,请回答: