题目内容
10.实验室制取某气体的化学方程式为:MnO2+4HCI(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCI2+X↑+2H2O,下列有关该反应的判断错误的是( )| A. | X的化学式为CI2 | |
| B. | 该反应涉及的物质中没有碱 | |
| C. | 该反应是置换反应 | |
| D. | 反应前后锰元素的化合价由+4价变为+2价 |
分析 A、由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式;
B、根据碱的定义解答;
C、根据置换反应的定义解答;
D、根据锰元素的化合价的变化解答.
解答 解:A、根据反应的化学方程式MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+X↑+2H2O,反应物中锰、氧、氢、氯原子个数分别为1、2、4、4,反应后的生成物中锰、氧、氢、氯原子个数分别为1、2、4、2,根据反应前后原子种类、数目不变,则每个X分子由2个氯原子构成,则物质X的化学式为Cl2,正确;
B、电离时产生的阴离子全部是氢氧根离子的化合物为碱,该反应涉及的物质中没有碱,正确;
C、置换反应是指由一种单质和一种化合物反应,生成另外一种单质和一种化合物的反应,该反应不是置换反应,错误;
D、反应前后锰元素的化合价由+4价变为+2价,正确;
故选C.
点评 本题难度不大,可依据已有的知识解答.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案
相关题目
20.高铁酸钾(K2FeO4)是一种新型高效净水处理剂,下列有关高铁酸钾的分析中,正确的是( )
| A. | 高铁酸钾是由三种元素组成 | |
| B. | 高铁酸钾中铁元素的化合价是+3价 | |
| C. | 高铁酸钾是一种有机物 | |
| D. | 高铁酸钾中铁元素的质量分数约为63.8% |
1.某植物培养液中含有NH4Cl和CuSO4,下列物质在该培养液中能大量共存的是( )
| A. | NaOH | B. | BaCl2 | C. | AgNO3 | D. | NaNO3 |
5.下列实验操作正确的是( )
| A. | 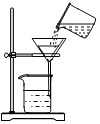 过滤 | B. | 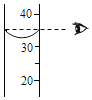 读取液体体积 | C. | 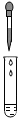 滴加液体 | D. | 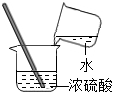 稀释浓硫酸 |
15.下列不属于溶液的是( )
| A. | 氨水 | B. | 澄清石灰水 | C. | 医药使用的碘酒 | D. | 蔗糖溶液 |
2.根据如图实验流程,下列分析正确的是( )
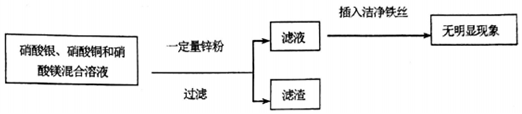

| A. | 滤液中一定有硝酸镁,可能有硝酸锌和硝酸亚铁 | |
| B. | 滤渣中一定有银和铜,可能有锌 | |
| C. | 滤渣中一定有银和铜,可能有镁 | |
| D. | 滤液中一定有硝酸镁和硝酸锌,可能有硝酸铜 |
7.将a g铁粉加到b g ZnSO4和 CuSO4的混合溶液中,充分反应后过滤,得到滤液和滤渣.下列有关说法中,不合理的是( )
| A. | 滤渣的质量一定大于a g,滤液的质量一定小于bg | |
| B. | 若滤渣中含有Fe,则滤液一定呈浅绿色 | |
| C. | 向滤渣中加入足量稀盐酸,滤渣全部溶解 | |
| D. | 若滤渣中只含有单质Cu,则滤液中至少含有两种金属阳离子 |
 如图是某元素的原子结构示意图及其在元素周期表中的部分信息.该元素是元素符号X应是Al,该元素相对原子质量的整数值为27,该元素的简单离子带3个正电荷的原因是原子核外的最外层上有3个电子.
如图是某元素的原子结构示意图及其在元素周期表中的部分信息.该元素是元素符号X应是Al,该元素相对原子质量的整数值为27,该元素的简单离子带3个正电荷的原因是原子核外的最外层上有3个电子.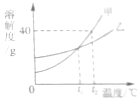 甲乙溶解度曲线如图所示
甲乙溶解度曲线如图所示