题目内容
9.实验室制取某些气体所需的装置如图所示,请回答下列问题: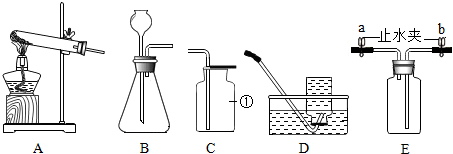
(1)实验仪器①的名称是集气瓶.
(2)实验室制取二氧化碳气体应选择的发生装置是B(填选项字母),反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.要检验二氧化碳,可将其通入到澄清的石灰水中,化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
(3)若用装置E收集较为纯净的氧气,瓶内先装满水,气体从a(填“a”或“b”)导管通入瓶内.若用装置E收集一瓶较纯净的二氧化碳气体,气体从b(填“a”或“b”)导管通入瓶内.
(5)若选A装置作为用高锰酸钾制取氧气的发生装置,还须补充的一种用品是棉花,写出该反应方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
分析 (1)据实验室常用仪器的认识解决;
(2)发生装置的选择要看反应物的状态和反应条件;据反应原理写出方程式;
(3)选择气体收集方法时通常考虑气体的密度和溶解性;
(4)用高锰酸钾制取氧气的发生装置试管口要有棉花团;据反应原理写出方程式.
解答 解:(1)依据实验室常用仪器的认识解决.答案为:集气瓶;
(2)实验室用大理石与稀盐酸制取二氧化碳,不需要加热,故制取二氧化碳气体应选择的发生装置是B,反应原理用化学方程式表示是CaCO3+2HCl═CaCl2+H2O+CO2↑.将二氧化碳通入澄清的石灰水中,生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
(3)若用装置E排水收集氧气,瓶内先装满水,气体从a导管通入瓶内;若用装置E收集一瓶较纯净的二氧化碳气体,因二氧化碳的密度比空气大,气体应长进短出,即从b入;
(4)制取时需要在试管口放一团棉花,它的作用是防止高锰酸钾粉末进入导管,造成导管堵塞;反应的方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
故答案为:
(1)集气瓶.
(2)B,CaCO3+2HCl═CaCl2+H2O+CO2↑.CO2+Ca(OH)2═CaCO3↓+H2O.
(3)a,b.(4)棉花,2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
点评 据反应物状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置,并掌握制取氧气、二氧化碳的方法,尤其是(3)能很好考查学生对知识的掌握和应用情况.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
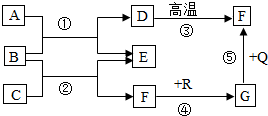 如图是初中化学中常见物质间的转化关系,其中,在通常情况下,F、G是组成元素相同的两种气体,Q、R都是黑色粉末,(部分反应条件和生成物略去).请回答:
如图是初中化学中常见物质间的转化关系,其中,在通常情况下,F、G是组成元素相同的两种气体,Q、R都是黑色粉末,(部分反应条件和生成物略去).请回答:
