题目内容
“温室效应”已经成为全球性环境问题,为减小和消除二氧化碳对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对二氧化碳创新利用的研究.
(1)法国化学家Paul Sabatier提出使CO2和H2在催化剂作用下生成CH4和H2O,试写出该反应的化学方程式______.
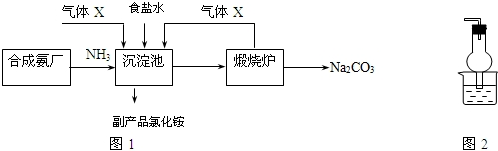
(2)我国早期纯碱生产的工艺流程可简要表示如下:
①上述生产纯碱过程中的副产品氯化铵在农业上的用途为______.
②沉淀池中发生的化学反应方程式是NaCl+H2O+NH3+X═NaHCO3↓+NH4Cl,其中X的化学式为______.
③实验中要向食盐水中先通入氨气再通入气体X,你认为原因是______.(填写字母)
A.氨气的密度比气体X小B.氨气极易溶于水,使溶液呈碱性后吸收更多的气体X通氨气的装置如图2所示,其干燥管的作用是______.
④煅烧炉中发生的分解反应的化学方程式为______,从上述流程中可得到可循环利用的物质是______.

解:(1)由题意CO2和H2在催化剂作用下生成CH4和H2O,该反应的化学方程式为CO2+4H2 CH4+2H2O.
CH4+2H2O.
(2)①氯化铵含有氮元素,属于氮肥,在农业上的用途是做氮肥;
②由质量守恒定律,根据反应前后,原子种类和数目均相等,可以确定X的化学式为CO2;
③由于氨气极易溶于水,为使溶液呈碱性后吸收更多的气体,故向食盐水中先通入氨气再通入气体X;氨气极易溶于水,易出现倒吸现象;图2装置中,在装置中都有相对较大的空间,这样可以防止倒吸现象的发生.
④煅烧炉中的物质是生成的NaHCO3,由题意结合质量守恒定律,故发生的分解反应的化学方程式为2NaHCO3═Na2CO3+CO2↑+H2O;由题意,从上述流程中可得到可循环利用的物质是CO2.
故答案为:
(1)CO2+4H2 CH4+2H2O
CH4+2H2O
(2)①做氮肥或肥料;②CO2;④③B;防倒吸;④2NaHCO3═Na2CO3+CO2↑+H2O,CO2(或二氧化碳)
分析:(1)根据题中所提示的反应物、生成物、反应条件写出该反应的化学方程式.
(2)吸收易溶性气体时,容易出现倒吸现象,可以通过特殊的装置来防止倒吸.由质量守恒定律,根据反应前后,原子种类和数目均相等,可以确定X的化学式.由于氨气极易溶于水的性质结合题目提供的信息分析判断.煅烧炉中的物质是生成的NaHCO3,由题意结合质量守恒定律,可以写出反应的化学方程式和找出可循环利用的物质.
点评:本题难度较大,主要考查学生信息处理能力、灵活运用所学知识解题的能力,题目增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
 CH4+2H2O.
CH4+2H2O.(2)①氯化铵含有氮元素,属于氮肥,在农业上的用途是做氮肥;
②由质量守恒定律,根据反应前后,原子种类和数目均相等,可以确定X的化学式为CO2;
③由于氨气极易溶于水,为使溶液呈碱性后吸收更多的气体,故向食盐水中先通入氨气再通入气体X;氨气极易溶于水,易出现倒吸现象;图2装置中,在装置中都有相对较大的空间,这样可以防止倒吸现象的发生.
④煅烧炉中的物质是生成的NaHCO3,由题意结合质量守恒定律,故发生的分解反应的化学方程式为2NaHCO3═Na2CO3+CO2↑+H2O;由题意,从上述流程中可得到可循环利用的物质是CO2.
故答案为:
(1)CO2+4H2
 CH4+2H2O
CH4+2H2O(2)①做氮肥或肥料;②CO2;④③B;防倒吸;④2NaHCO3═Na2CO3+CO2↑+H2O,CO2(或二氧化碳)
分析:(1)根据题中所提示的反应物、生成物、反应条件写出该反应的化学方程式.
(2)吸收易溶性气体时,容易出现倒吸现象,可以通过特殊的装置来防止倒吸.由质量守恒定律,根据反应前后,原子种类和数目均相等,可以确定X的化学式.由于氨气极易溶于水的性质结合题目提供的信息分析判断.煅烧炉中的物质是生成的NaHCO3,由题意结合质量守恒定律,可以写出反应的化学方程式和找出可循环利用的物质.
点评:本题难度较大,主要考查学生信息处理能力、灵活运用所学知识解题的能力,题目增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案
相关题目
 能源与环境已成为人们关注的热点.
能源与环境已成为人们关注的热点.