题目内容
5.从C、H、O、N、S、P、Na、Ba等8种元素中选择恰当的元素,用离子符号、化学式或化学方程式按下列要求填空:(1)硫酸钠中的阴离子SO42-;氯化亚铁中的阳离子Fe2+;溶于水后显酸性的气体CO2;用于生产玻璃、洗涤剂的盐Na2CO3.
(2)一种暗红色的固体燃烧生成大量的白烟4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(3)有沉淀生成的中和反应H2SO4+Ba(OH)2═BaSO4↓+2H2O.
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答 解:(1)硫酸钠中的阴离子是硫酸根离子,其离子符号为:SO42-.故填:SO42-;
根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;氯化亚铁中的阳离子为亚铁离子表示为:Fe2+;故填:Fe2+;
二氧化碳溶于水,并与水反应生成碳酸,显酸性,故填:CO2;
碳酸钠在工业上用于生产玻璃、洗涤剂,属于盐,故填:Na2CO3
(2)红磷为暗红色和氧气在点燃的条件下生成五氧化二磷白色固体,故答案为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(3)硫酸属于酸,氢氧化钡属于碱,两者发生中和反应生成硫酸钡沉淀和水,符合题意,反应的化学方程式为:H2SO4+Ba(OH)2═BaSO4↓+2H2O.
故填:H2SO4+Ba(OH)2═BaSO4↓+2H2O.
点评 本题难度不大,主要考查同学们对常见化学用语(化学式、离子符号、化学方程式等)的书写和理解能力.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
4.下列实验现象描述正确的是( )
| A. | 氢气在空气中燃烧产生淡蓝色火焰 | |
| B. | 红磷在空气中燃烧,产生白雾 | |
| C. | 铁在纯氧中剧烈燃烧、火星四射,生成四氧化三铁 | |
| D. | 木炭在氧气中完全燃烧,生成能使澄清石灰水变浑浊的二氧化碳气体 |
9.下列现象的描述不正确的是( )
| A. | 往食盐中加水,食盐逐渐减少,水变咸了 | |
| B. | 蜡烛燃烧时,可观察到蜡烛熔化,发光发热,伴随有少量黑烟 | |
| C. | 烧开水的过程中可观察到有气泡产生 | |
| D. | 人呼吸产生的气体中有二氧化碳 |
10.碳酸镁晶须(MgCO3•nH2O,n=1-5的整数)广泛应用于冶金、耐火材料及化工产品等领域.为测定碳酸镁晶须中n的值,学习小组设计了如下装置并进行实验:(不考虑稀盐酸挥发)
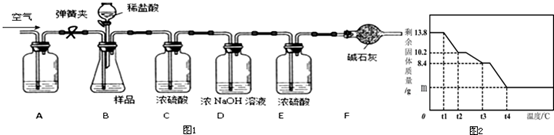
【查阅资料】:碳酸镁晶须受热分解,生成3种氧化物;
【实验步骤】①组装仪器,检查装置的气密性;②准确称取3.45g MgCO3•nH2O放在B装置中,连接仪器;③打开弹簧夹,鼓入一段时间空气,称量B、C、D、E、F装置的质量;④关闭弹簧夹,打开分液漏斗活塞,缓缓滴入稀盐酸至无气泡产生为止;⑤打开弹簧夹,鼓入一段时间空气;
⑥准确称量B、C、D、E、F装置的质量(如下表);
⑦根据数据进行计算.
【实验分析及数据处理】
(1)完善实验步骤:①检查装置的气密性;⑤鼓入一段时间空气;
(2)请计算碳酸镁晶须中的n值.(要求有计算过程,3分)
(3)A装置中盛放的溶液是NaOH(浓)溶液;
【实验反思】
(4)下列选项中,会造成实验结果偏大的是①⑤;偏小的是②③⑥;
①反应结束后,没有通空气;②滴入稀盐酸前,没有通空气;③没有A装置; ④D装置中NaOH溶液浓度过大;⑤稀盐酸滴加速率太快; ⑥没有C装置;
(5)为精确测定n的值,在老师指导下,小组同学称取13.8g MgCO3•nH2O进行热重分析,并绘制出如图所示的热重曲线示意图.则:
①t1℃至t2℃时,剩余固体质量不变的原因为没有达到该晶分解需要的温度;
②t1℃至t2℃时MgCO3•nH2O分解的化学方程式为:MgCO3•3H2O═MgCO3•H2O+2H2O;
③完全反应后,剩余固体的质量m为4g.

【查阅资料】:碳酸镁晶须受热分解,生成3种氧化物;
【实验步骤】①组装仪器,检查装置的气密性;②准确称取3.45g MgCO3•nH2O放在B装置中,连接仪器;③打开弹簧夹,鼓入一段时间空气,称量B、C、D、E、F装置的质量;④关闭弹簧夹,打开分液漏斗活塞,缓缓滴入稀盐酸至无气泡产生为止;⑤打开弹簧夹,鼓入一段时间空气;
| B | C | D | E | F | |
| 反应前 | 122.0g | 250.0g | 300.0g | 350.0g | 330.0g |
| 反应后 | 120.6g | 250.2g | 301.0g | 350.1g | 332.0g |
⑦根据数据进行计算.
【实验分析及数据处理】
(1)完善实验步骤:①检查装置的气密性;⑤鼓入一段时间空气;
(2)请计算碳酸镁晶须中的n值.(要求有计算过程,3分)
(3)A装置中盛放的溶液是NaOH(浓)溶液;
【实验反思】
(4)下列选项中,会造成实验结果偏大的是①⑤;偏小的是②③⑥;
①反应结束后,没有通空气;②滴入稀盐酸前,没有通空气;③没有A装置; ④D装置中NaOH溶液浓度过大;⑤稀盐酸滴加速率太快; ⑥没有C装置;
(5)为精确测定n的值,在老师指导下,小组同学称取13.8g MgCO3•nH2O进行热重分析,并绘制出如图所示的热重曲线示意图.则:
①t1℃至t2℃时,剩余固体质量不变的原因为没有达到该晶分解需要的温度;
②t1℃至t2℃时MgCO3•nH2O分解的化学方程式为:MgCO3•3H2O═MgCO3•H2O+2H2O;
③完全反应后,剩余固体的质量m为4g.
17.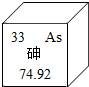 2014年3月24日,央视财经《经济半小时》曝光:湖南石门河砷超标1000多倍,需要长期进行砷污染土壤修复研究工作,在元素周期表中砷元素的某些信息如图所示,下列有关砷的说法错误的是( )
2014年3月24日,央视财经《经济半小时》曝光:湖南石门河砷超标1000多倍,需要长期进行砷污染土壤修复研究工作,在元素周期表中砷元素的某些信息如图所示,下列有关砷的说法错误的是( )
 2014年3月24日,央视财经《经济半小时》曝光:湖南石门河砷超标1000多倍,需要长期进行砷污染土壤修复研究工作,在元素周期表中砷元素的某些信息如图所示,下列有关砷的说法错误的是( )
2014年3月24日,央视财经《经济半小时》曝光:湖南石门河砷超标1000多倍,需要长期进行砷污染土壤修复研究工作,在元素周期表中砷元素的某些信息如图所示,下列有关砷的说法错误的是( )| A. | 砷是一种高毒性的非金属元素 | |
| B. | 砷元素的原子核内质子数为33 | |
| C. | 砷元素的相对原子质量为74.92 | |
| D. | 砒霜的主要成分为三氧化二砷,其中砷元素化合价为-3 |
15.下列各组物质完全反应后,溶液的总质量增加的是( )
| A. | 铁和稀硫酸 | B. | 铁和硫酸铜溶液 | ||
| C. | 碳酸钠溶液和稀硫酸 | D. | 硫酸铜溶液和氢氧化钠溶液 |
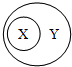 下列选项符合图示包含关系的是( )
下列选项符合图示包含关系的是( )