题目内容
根据如图所示,回答有关问题:
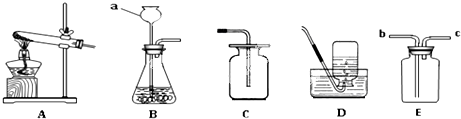
(1)写出图中标有字母的仪器名称:a .
(2)实验室用高锰酸钾制取氧气,应选用的发生装置是 (填字母),实验时该装置试管口应放一团棉花,其目的是 ;反应的化学方程式为 .D装置可用来收集氧气的原因是 .
(3)欲使用装置E用排空气法收集氧气,则气体应从 (填“b”或“c”)端通入;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从 (填“b”或“c”)端通入.
(4)实验室常用在过氧化氢的溶液中加入少量的二氧化锰来制取氧气,写出反应的化学方程式: ;应选用的发生装置是 .
(5)小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂.
【完成实验】按下表进行实验,并测定分解温度(分解温度越低,催化效果越好).
【分析数据、得出结论】
①由实验 (填实验编号)与实验④对比,证明猜想合理;
②实验所用的三种物质,催化效果最好的是 .
【反思】
③若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后的质量和 不变.
(6)实验室常用无水醋酸钠和碱石灰两种固体混合物加热制取甲烷气体.甲烷的密度比空气密度小,极难溶于水,制取甲烷的发生装置是 ,收集装置可用 .

(1)写出图中标有字母的仪器名称:a
(2)实验室用高锰酸钾制取氧气,应选用的发生装置是
(3)欲使用装置E用排空气法收集氧气,则气体应从
(4)实验室常用在过氧化氢的溶液中加入少量的二氧化锰来制取氧气,写出反应的化学方程式:
(5)小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂.
【完成实验】按下表进行实验,并测定分解温度(分解温度越低,催化效果越好).
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | 氯酸钾 | 580 |
| ② | 氯酸钾、二氧化锰(质量比1:1) | 350 |
| ③ | 氯酸钾、氧化铜(质量比1:1) | 370 |
| ④ | 氯酸钾、氧化铁(质量比1:1) | 390 |
①由实验
②实验所用的三种物质,催化效果最好的是
【反思】
③若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后的质量和
(6)实验室常用无水醋酸钠和碱石灰两种固体混合物加热制取甲烷气体.甲烷的密度比空气密度小,极难溶于水,制取甲烷的发生装置是
考点:氧气的制取装置,氧气的收集方法,制取氧气的操作步骤和注意点,催化剂的特点与催化作用,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)熟悉常见仪器,了解名称;
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气;为了防止高锰酸钾进入导管,应该在试管口塞一团棉花;氧气不易溶于水,密度比空气大;
(3)不同的实验装置,功能不同;
(4)用过氧化氢溶液制取氧气,通常加入二氧化锰作催化剂,同时生成水,据此书写方程式;该反应不需加热,故选发生装置B;
(5)①根据对照试验要求只有一个变量,其他条件都相同进行分析回答;
②根据分解时所需温度最低的,催化效果越好进行分析;
③催化剂是指在化学反应里能改变其他物质的化学反应速率(既能提高也能降低),而本身的质量和化学性质在化学反应前后都没有发生改变的物质.故要证明Fe203是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质不变.
(6)题目最后给出有关甲烷气体的信息,根据这些信息选择甲烷的发生装置和收集装置.
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气;为了防止高锰酸钾进入导管,应该在试管口塞一团棉花;氧气不易溶于水,密度比空气大;
(3)不同的实验装置,功能不同;
(4)用过氧化氢溶液制取氧气,通常加入二氧化锰作催化剂,同时生成水,据此书写方程式;该反应不需加热,故选发生装置B;
(5)①根据对照试验要求只有一个变量,其他条件都相同进行分析回答;
②根据分解时所需温度最低的,催化效果越好进行分析;
③催化剂是指在化学反应里能改变其他物质的化学反应速率(既能提高也能降低),而本身的质量和化学性质在化学反应前后都没有发生改变的物质.故要证明Fe203是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质不变.
(6)题目最后给出有关甲烷气体的信息,根据这些信息选择甲烷的发生装置和收集装置.
解答:解:(1)图中a是用于添加液体的长颈漏斗.
故答案为:长颈漏斗;
(2)高锰酸钾是固体需加热才能产生氧气,所以选择固体加热装置;收集氧气因为氧气密度大于空气密度可选用向上排空气法,氧气不易溶于水,所以可选用排水法收集;高锰酸钾加热生成锰酸钾、二氧化锰和氧气.
故答案为:A;防止加热时高锰酸钾进入导气管;2KMnO
K2MnO4+MnO2+O2↑;氧气难溶于水.
(3)欲使用装置E用排空气法收集氧气,因为氧气的密度比空气大,则氧气应从b端通入;
欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从c端通入.
故答案为:b;c.
(4)用过氧化氢溶液制取氧气,通常加入二氧化锰作催化剂,同时生成水,方程式是2H2O2
2H2O+O2↑;该反应不需加热,故选发生装置B.
故答案是:2H2O2
2H2O+O2↑;B;
(5)①根据催化剂能改变化学反应的速率,可选择加催化剂和不加催化剂的进行比较分解温度即可,要想证明除Mn02、CuO外,Fe203也可以作KCl03分解的催化剂,可选择实验①和实验④对比,证明猜想合理.
故答案是:①
②分解时所需温度最低的,催化效果越好.
故答案是:二氧化锰;
③催化剂是指在化学反应里能改变其他物质的化学反应速率(既能提高也能降低),而本身的质量和化学性质在化学反应前后都没有发生改变的物质.故要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质不变.
故答案是:质量不变;
(6)由信息:实验室常用无水醋酸钠和碱石灰两种固体混合物加热制取甲烷气体,可知制取甲烷的发生装置应选A;
信息:甲烷的密度比空气密度小,极难溶于水,说明甲烷可采取装置C排水法收集,也可以采取装置D向下排空气法收集.
故答案为:A;C或D.
故答案为:长颈漏斗;
(2)高锰酸钾是固体需加热才能产生氧气,所以选择固体加热装置;收集氧气因为氧气密度大于空气密度可选用向上排空气法,氧气不易溶于水,所以可选用排水法收集;高锰酸钾加热生成锰酸钾、二氧化锰和氧气.
故答案为:A;防止加热时高锰酸钾进入导气管;2KMnO
| ||
(3)欲使用装置E用排空气法收集氧气,因为氧气的密度比空气大,则氧气应从b端通入;
欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从c端通入.
故答案为:b;c.
(4)用过氧化氢溶液制取氧气,通常加入二氧化锰作催化剂,同时生成水,方程式是2H2O2
| ||
故答案是:2H2O2
| ||
(5)①根据催化剂能改变化学反应的速率,可选择加催化剂和不加催化剂的进行比较分解温度即可,要想证明除Mn02、CuO外,Fe203也可以作KCl03分解的催化剂,可选择实验①和实验④对比,证明猜想合理.
故答案是:①
②分解时所需温度最低的,催化效果越好.
故答案是:二氧化锰;
③催化剂是指在化学反应里能改变其他物质的化学反应速率(既能提高也能降低),而本身的质量和化学性质在化学反应前后都没有发生改变的物质.故要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质不变.
故答案是:质量不变;
(6)由信息:实验室常用无水醋酸钠和碱石灰两种固体混合物加热制取甲烷气体,可知制取甲烷的发生装置应选A;
信息:甲烷的密度比空气密度小,极难溶于水,说明甲烷可采取装置C排水法收集,也可以采取装置D向下排空气法收集.
故答案为:A;C或D.
点评:装置选取、反应方程式的书写,是考试的重要考查点,此外,氧气的收集及实验中的注意事项也是常考的内容,因此,同学们要加强对知识的理解,才能灵活应用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
如图是实验室制取二氧化碳气体,并试验其化学性质的装置图,若产生的二氧化碳足量,试根据装置图填写下面的实验记录:
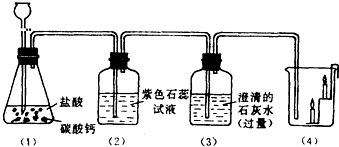

| 实验项目 | 实现现象 | (1)-(3)写化学方程式、(4)写结论 |
| (1) | 1 | |
| (2) | 11 | |
| (3) | 1 | |
| (4) | 1 |
下列实验操作不正确的是( )
| A、给试管内液体加热时,试管口不要对着人 |
| B、实验要节约药品,实验剩余的药品要放回原瓶 |
| C、取液后的试管,应保持橡胶帽在上,不要平放或倒置 |
| D、利用托盘天平称量物质的质量,一般准确到0.1g |
前者属于化合物后者属于单质的是( )
| A、空气、蒸馏水 |
| B、二氧化碳、氢气 |
| C、磷、冰 |
| D、食盐水、氧气 |
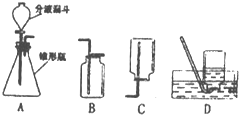 过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解,分液漏斗可以通过调节活塞控制液体的滴加速度,请根据如图回答以下问题:
过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解,分液漏斗可以通过调节活塞控制液体的滴加速度,请根据如图回答以下问题: