题目内容
17.下列关于实验现象的描述正确的是( )| A. | 硫在氧气中燃烧生成二氧化硫 | |
| B. | 白磷在空气中燃烧产生浓厚的白雾 | |
| C. | 带锈铁钉放入稀盐酸中,溶液由无色变成浅绿色 | |
| D. | 电解水实验中,正极与负极产生的气体的体积比约为1:2 |
分析 根据硫燃烧的现象、白磷燃烧生成五氧化二磷固体、盐酸与氧化铁反应生成氯化铁水溶液的颜色以及电解水的知识进行分析解答.
解答 解:A、硫在氧气中燃烧生成二氧化硫,是实验的结论,不是实验现象,错误;
B、白磷在空气中燃烧产生浓厚的白烟,不是白雾,错误;
C、带锈铁钉放入稀盐酸中,生成氯化铁,溶液由无色变成黄色,错误;
D、电解水实验中,正极与负极产生的气体的体积比约为1:2,正确;
故选D.
点评 本题考查的是常见的实验现象,完成此题,可以依据已有的知识进行.注意白烟和白雾的区别.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
8.下列物质属于非金属单质的是( )
| A. | 水 | B. | 二氧化碳 | C. | 金刚石 | D. | 铜 |
5.如图图象中有关量的变化趋势与对应叙述关系正确的是( )
| A. |  向氢氧化钠和碳酸钠的混合物中滴加盐酸至过量 向氢氧化钠和碳酸钠的混合物中滴加盐酸至过量 | |
| B. |  向一定质量的稀硫酸中滴加水 向一定质量的稀硫酸中滴加水 | |
| C. | 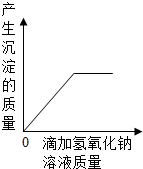 向氯化铁的混合溶液中滴加氢氧化钠溶液至过量 向氯化铁的混合溶液中滴加氢氧化钠溶液至过量 | |
| D. | 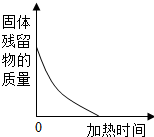 高温煅烧一定质量的石灰石 高温煅烧一定质量的石灰石 |
9.最适宜在实验室里制取氢气的一组原料是( )
| A. | 铁和稀硫酸 | B. | 锌和稀硫酸 | C. | 镁和浓盐酸 | D. | 大理石和稀盐酸 |
 如图所示,请回答下列问题:
如图所示,请回答下列问题: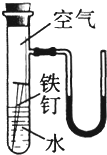 请回答下列有关金属的问题.
请回答下列有关金属的问题.