题目内容
15.某钢铁厂每天需要消耗4000t含Fe2O380%的赤铁矿石,计算该钢铁厂理论上可日产Fe97%的生铁质量是多少?(结果保留到0.1)分析 由赤铁矿石的质量、氧化铁的质量分数、生铁中铁的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出炼出生铁的质量.
解答 解:设日产生铁的质量为x
Fe2O3 的质量为:4000t×80%=3200t
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
3200t 97%x
$\frac{160}{112}=\frac{3200t}{97%x}$ 解得 x=2309.3t
答:日产生铁的质量是2309.3t
点评 本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.小刘同学想在实验室里用NaOH溶液来制取Na2CO3溶液.
【查阅资料】①CO2通入NaOH溶液时极易因CO2过量而产生NaHCO3,且无明显现象.
②NaHCO3溶液煮沸时不会发生分解.
③NaHCO3+NaOH=Na2CO3+H2O
④Ca(HCO3)2可溶于水
【制取步骤】①量取两份50mL相同浓度的NaOH溶液备用;
②用一份50mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
③小心煮沸②溶液1-2分钟;
④在得到的③的溶液中加入另一份50mL NaOH溶液,使其充分混合即得.
【实验探究】为了检验制得的溶液是否为纯净的Na2CO3溶液,请你与小刘同学一起完成下列实验探究:
【结论】所制得的溶液为纯净的Na2CO3溶液.
【评价与反思】有人认为实验步骤的顺序对调,即先混合,再煮沸,更合理.你认为对吗?请说明理由:不对,在煮沸之前溶液中含有未参与反应的二氧化碳气体,如果先混合,则氢氧化钠溶液会和溶液中的二氧化碳继续反应,导致制备的碳酸钠不纯净.
【查阅资料】①CO2通入NaOH溶液时极易因CO2过量而产生NaHCO3,且无明显现象.
②NaHCO3溶液煮沸时不会发生分解.
③NaHCO3+NaOH=Na2CO3+H2O
④Ca(HCO3)2可溶于水
【制取步骤】①量取两份50mL相同浓度的NaOH溶液备用;
②用一份50mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
③小心煮沸②溶液1-2分钟;
④在得到的③的溶液中加入另一份50mL NaOH溶液,使其充分混合即得.
【实验探究】为了检验制得的溶液是否为纯净的Na2CO3溶液,请你与小刘同学一起完成下列实验探究:
| 实验步骤 | 实验现象 | 实验结论 | |
| 取少量制得的溶液于试管中,加入过量的CaCl2溶液 | 产生白色沉淀 | 原来制得的溶液中含有Na2CO3 | |
| 将上步实验所得混合物进行过滤,将滤液分成两份 | 取其中一份加入足量的稀盐酸 | 无气泡产生 | 原来制得的溶液中不含碳酸氢钠 |
| 取另一份加入MgCl2溶液 | 无明显现象 | 原来制得的溶液中不含NaOH | |
【评价与反思】有人认为实验步骤的顺序对调,即先混合,再煮沸,更合理.你认为对吗?请说明理由:不对,在煮沸之前溶液中含有未参与反应的二氧化碳气体,如果先混合,则氢氧化钠溶液会和溶液中的二氧化碳继续反应,导致制备的碳酸钠不纯净.
3.人们在认识事物时可以采取多种方法,多种角度,下面对硝酸认识不正确的是( )
| A. | 硝酸铵是一种氮肥 | B. | 硝酸铵是一种氧化物 | ||
| C. | 硝酸铵中氮元素的化合价不同 | D. | 硝酸铵属于盐类 |
10.下列对宏观现象的微观解释不正确的是( )
| A. | 温度计受热时水银柱上升,是因为受热时汞原子之间的间隔变大 | |
| B. | 溶液能够导电的原因是溶液中有大量能够自由移动的离子 | |
| C. | 稀盐酸和稀硫酸都能使紫色石蕊溶液变红,是因为它们溶液中都含H+ | |
| D. | 氯化钠溶于水是由于构成氯化钠的分子均匀分散到水中 |
7.化学学科的思维方法有多种,其中推理是最常见的一种思维方法.以下推理正确的是( )
| A. | 酸溶液中一定含有氢离子,含有氢离子的溶液一定是酸溶液 | |
| B. | 有机物一定含有碳元素,含有碳元素的化合物不一定是有机化合物 | |
| C. | 氧化物由氧元素和另一种元素组成,则仅含氧元素及另一种元素的物质一定是氧化物 | |
| D. | 铁和银均为金属,铁与稀盐酸反应生成氢气,则银也能与稀盐酸反应生成氢气 |
5.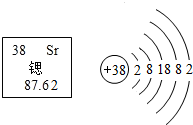 据媒体报道,锶晶体格钟是一种新型原子钟,其准确度高得惊人,它能在50亿年间不慢一秒也不快一秒.如图为锶元素的相关信息,下列说法正确的是( )
据媒体报道,锶晶体格钟是一种新型原子钟,其准确度高得惊人,它能在50亿年间不慢一秒也不快一秒.如图为锶元素的相关信息,下列说法正确的是( )
 据媒体报道,锶晶体格钟是一种新型原子钟,其准确度高得惊人,它能在50亿年间不慢一秒也不快一秒.如图为锶元素的相关信息,下列说法正确的是( )
据媒体报道,锶晶体格钟是一种新型原子钟,其准确度高得惊人,它能在50亿年间不慢一秒也不快一秒.如图为锶元素的相关信息,下列说法正确的是( )| A. | 原子核内中子数为87 | B. | 该元素的原子序数为38 | ||
| C. | 锶离子Sr2+中有38个电子 | D. | 锶属于非金属元素,位于第五周期 |