题目内容
5.如图是初中化学常见的实验装置,请结合所学化学知识,回答有关问题: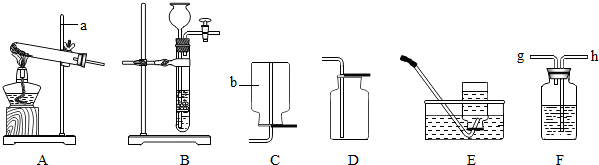
(1)气体的制取装置:
①写出带有标号仪器的名称:a铁架台、b集气瓶.
②用KClO3和MnO2制取O2应选用的发生装置是A(填序号,下同);用稀硫酸和锌粒制取H2应选用的收集装置是C或E.
(2)气体的制取原理:
①实验室用过氧化氢溶液和二氧化锰混合制取氧气,其中二氧化锰起催化作用,该反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
②实验室制取二氧化碳的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)气体的净化和检验:
①实验制取的O2中含有水蒸气,若使用F装置对氧气进行干燥,则装置内放入的药品是浓硫酸,气体应从h端(填字母“g”或“h”)通入.
②若要探究所得二氧化碳气体中是否含有挥发出来的HCl气体,可将生成的气体通入硝酸银溶液中.
分析 铁架台是常用的夹持仪器,集气瓶是收集气体的仪器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.浓硫酸可以干燥氧气,并且长进短出;若要探究所得二氧化碳气体中是否含有挥发出来的HCl气体,可将生成的气体通入硝酸银溶液中,观察是否有白色沉淀生成.
解答 解:(1)铁架台是常用的夹持仪器,集气瓶是收集气体的仪器,如果用氯酸钾制氧气就需要加热,实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;故答案为:①铁架台;集气瓶;②A;C;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,其中二氧化锰起催化作用;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;故答案为:①催化;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;②CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)浓硫酸可以干燥氧气,并且长进短出;若要探究所得二氧化碳气体中是否含有挥发出来的HCl气体,可将生成的气体通入硝酸银溶液中,观察是否有白色沉淀生成;故答案为:①浓硫酸;h;②硝酸银;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,气体的干燥和检验等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 金刚石很硬,用作钻探机的钻头 | |
| B. | 用碳素墨水写文字档案,便于长期保存 | |
| C. | 火碱具有碱性,故可用于改良酸性土壤 | |
| D. | 镁粉燃烧发出耀眼白光,可用于制作照明弹 |
| A. | 是一种碳单质 | B. | 含有碳元素和铝元素 | ||
| C. | 具有导电性 | D. | 具有可燃性 |
| 物质 | X | Y | M | N |
| 反应前物质质量/g | 1.7 | 2.2 | 7.9 | 0.9 |
| 反应后物质质量/g | m | 6.6 | 0 | 2.7 |
| A. | m 的值为1.7 | |
| B. | 物质X可能为催化剂 | |
| C. | 参加化学变化的物质Y、N的质量比为22:9 | |
| D. | 该反应一定是高锰酸钾分解制氧气 |
| A. | 青蒿素是一种有机高分子化合物 | |
| B. | 青蒿素中碳、氧元素个数比为3:1 | |
| C. | 青蒿素中氢元素的质量分数最小 | |
| D. | 青蒿素由15个碳原子、22个氢原子和5个氧原子构成 |

 某学习小组的同学以盖房子的游戏来建立几种重要物质之间的联系,如图,游戏规则是上、下相邻的物质间均可发生反应.
某学习小组的同学以盖房子的游戏来建立几种重要物质之间的联系,如图,游戏规则是上、下相邻的物质间均可发生反应.