题目内容
4.将60g K2CO3溶液与108.7g BaCl2溶液混合,恰好完全反应.过滤后所得滤液的质量为149g.则:(1)反应生成沉淀的质量19.7 g.
(2)所得滤液中溶质的质量分数10%.
分析 根据反应前后的质量差即为生成沉淀碳酸钡的质量,根据碳酸钡的质量可以计算反应生成氯化钾的质量,进一步可以计算所得滤液中溶质的质量分数进行分析.
解答 解:(1)反应生成的沉淀碳酸钡的质量为:60g+108.7g-149g=19.7g,
答:生成沉淀的质量为19.7g;
(2)设生成氯化钾的质量为x,
K2CO3+BaCl2=2KCl+BaCO3↓,
149 197
x 19.7g
$\frac{149}{x}$=$\frac{197}{19.7g}$
x=14.9g
所得滤液中溶质的质量分数为:$\frac{14.9g}{149g}$×100%×100%=10%,
答:氯化钾的质量分数为:10%.
故答案为:(1)19.7;
(2)10%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
14.2009年12月份的哥本哈根气候会议的议程中非常重要的一项就是如何有效控制温室效应,降低碳排放;在前不久召开的十一届全国人大三次会议上,各地人大代表也提出“低碳经济,低碳生活”,下列行为中你认为能减少碳排放的是( )
| A. | 开私家车出去春游 | |
| B. | 野炊时将垃圾和未使用完的柴火焚烧 | |
| C. | 使用太阳能热水器淋浴 | |
| D. | 使用纸巾代替手帕 |
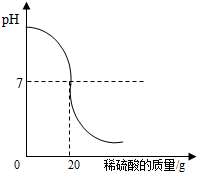 为了测定某氢氧化钠溶液中溶质的质量分数,取氢氧化钠溶液50g,向其中加入溶质的质量分数为4.9%的稀硫酸,加入稀硫酸质量与pH的变化情况如图所示.计算:当加入稀硫酸质量为20g时,所得溶液中溶质的质量分数.
为了测定某氢氧化钠溶液中溶质的质量分数,取氢氧化钠溶液50g,向其中加入溶质的质量分数为4.9%的稀硫酸,加入稀硫酸质量与pH的变化情况如图所示.计算:当加入稀硫酸质量为20g时,所得溶液中溶质的质量分数.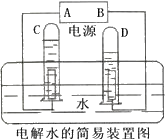 如图是电解水的简易装置.
如图是电解水的简易装置.