题目内容
17. 在初中化学中,我们学习了溶液的有关知识.右图是KNO3的溶解度曲线.
在初中化学中,我们学习了溶液的有关知识.右图是KNO3的溶解度曲线.(1)从如图溶解度曲线可以得到的信息是(写一条)20℃时,硝酸钾的溶解度是31.6g.
(2)小明参照右图在常温20℃时进行了如图实验:
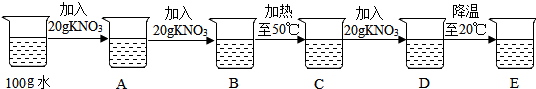
小明观察到A中所加固体全部溶解,则B中的现象是固体部分溶解.
上述实验过程中属于不饱和溶液的是(填字母)ACD.
现需配制24%的硝酸钾溶液,则霈要控制的温度范围是≥20℃.
分析 根据题目信息和溶解度曲线可知:硝酸钾固体物质的溶解度,是随温度升高而增大;20℃时,硝酸钾的溶解度是31.6g;小明观察到A中所加固体全部溶解,则B中的现象是:固体部分溶解,因为在该温度下,硝酸钾的溶解度是31.6g;上述实验过程中属于不饱和溶液的是:ACD;现需配制24%的硝酸钾溶液,则需要控制的温度范围是:≥20℃,因为$\frac{31.6g}{131.6g}×100%≈24%$.
解答 解:(1)由溶解度曲线可知:硝酸钾固体物质的溶解度,是随温度升高而增大;20℃时,硝酸钾的溶解度是31.6g;故答案为:20℃时,硝酸钾的溶解度是31.6g;
(2)小明观察到A中所加固体全部溶解,则B中的现象是:固体部分溶解,因为在该温度下,硝酸钾的溶解度是31.6g;上述实验过程中属于不饱和溶液的是:ACD;现需配制24%的硝酸钾溶液,则需要控制的温度范围是:≥20℃,因为$\frac{31.6g}{131.6g}×100%≈24%$;故答案为:固体部分溶解;ACD;≥20℃;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
5.某纯净物M燃烧的化学方程式为:M+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+2H2O,则M的化学式是( )
| A. | C2H2 | B. | C2H4 | C. | C2H6 | D. | C2H4O |
2.Fenton法常用于处理含难降解有机物的工业废水.其原理利用Fe2+和H2O2的反应产生能降解污染物的活性成分.现运用该方法降解有机污染物p-CP,探究有关因素对降解反应速率的影响.
实验探究:控制p-CP的初始浓度相同,实验温度恒定在25℃或40℃(其余实验条件见表),设计如下对比试验.
(1)请完成以下实验设计表(表中不要留空格).
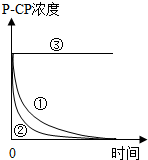
实验测得p-CP的浓度随时间变化的关系如图.
(2)实验①、②表明温度升高,降解反应速率加快.实验发现,温度过高时,降解反应较难发生.请从Fenton法所用试剂H2O2的角度分析原因:过氧化氢在温度过高时易分解.
(3)实验③得出的结论是:pH等于10时,反应速率趋向于零.
(4)为测定不同时间内有机物降解的浓度,需在不同时间从反应器中取样,并使所取样品中的降解反应立即停止下来.根据如图中的信息,给出一种迅速停止反应的方法:将所取样品迅速加入到一定量的NaOH溶液中,使pH为10.
实验探究:控制p-CP的初始浓度相同,实验温度恒定在25℃或40℃(其余实验条件见表),设计如下对比试验.
(1)请完成以下实验设计表(表中不要留空格).
| 实验编号 | 实验目的 | 温度/ | pH | 浓度/(mg.L-1) | |
| ① | 为提供参照 | 25 | 3 | H2O2 | Fe2+ |
| ② | 探究温度对降解反应速率的影响 | 204 | 16.8 | ||
| ③ | 25 | 10 | 204 | 16.8 | |
(2)实验①、②表明温度升高,降解反应速率加快.实验发现,温度过高时,降解反应较难发生.请从Fenton法所用试剂H2O2的角度分析原因:过氧化氢在温度过高时易分解.
(3)实验③得出的结论是:pH等于10时,反应速率趋向于零.
(4)为测定不同时间内有机物降解的浓度,需在不同时间从反应器中取样,并使所取样品中的降解反应立即停止下来.根据如图中的信息,给出一种迅速停止反应的方法:将所取样品迅速加入到一定量的NaOH溶液中,使pH为10.

9.学校午餐食谱:米饭、鱼、油煎鸡蛋,为使营养均衡,你认为应补充( )
| A. | 红烧肉 | B. | 牛奶 | C. | 油条 | D. | 黄瓜 |
6.在①合金、黄铁矿、石油、纯碱 ②N2、P、Mg、O2 ③Al2O3、Fe3O4、CuO、SO2三组物质中,每组有一种物质在分类上与其他物质不同,这三种物质分别是( )
| A. | 纯碱、Mg、SO2 | B. | 黄铁矿、Mg、Al2O3 | C. | 合金、O2、Fe3O4 | D. | 纯碱、P、SO2 |
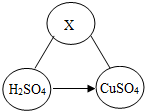 H2SO4、X、CuSO4三种物质存在一定关系如图所示(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应).
H2SO4、X、CuSO4三种物质存在一定关系如图所示(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应).
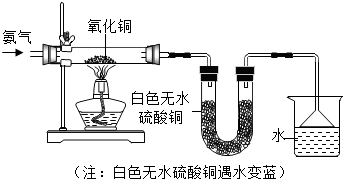
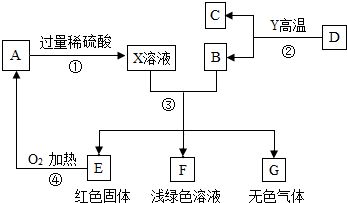 A、B、C、D、E、F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,它们之间的相互转化关系如下图所示:
A、B、C、D、E、F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,它们之间的相互转化关系如下图所示: