题目内容
2.在生产、生活中处处都涉及到化学知识.请回答:(1)炼铁厂常以焦炭、赤铁矿石(主要成分是Fe2O3)、空气等为主要原料炼铁,请写出一氧化碳与氧化铁在高温下反应的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)每年全世界钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失.请你写出一种防止铁锅生锈的方法:保持洁净与干燥.
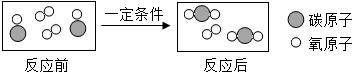
(3)下图表示自来水消毒过程中发生的一个反应的微观过程:

①写出上述物质中单质的化学式Cl2;②物质D中氯元素的化合价为+1价.
(4)电器着火时常使用干粉灭火器灭火,干粉的主要成分是碳酸氢钠,受热后生成一种碳酸盐和两种氧化物,请写出该反应的化学方程式:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
分析 (1)一氧化碳与氧化铁在高温下反应生成铁和二氧化碳,写出反应的化学方程式即可.
(2)铁与水、氧气充分接触时容易生锈,使铁制品与氧气和水隔绝可以防止生锈,进行分析解答.
(3)①根据B分子的构成可知B的化学式;
②根据化合物中元素化合价的代数和为0分析计算.
(4)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)一氧化碳与氧化铁在高温下反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)铁与氧气和水充分接触时容易生锈,防止铁锅生锈,最简单的方法是保持洁净与干燥(合理即可).
(3)①B分子的构成可知B的化学式为:Cl2;
②D的化学式为HClO,设HClO中Cl的化合价为x
则(+1)+x+(-2)=0
解得x=+1;
(4)碳酸氢钠(NaHCO3)受热分解生成碳酸钠、水和一种能灭火的气体(由质量守恒定律,反应前后元素种类不变,该气体是二氧化碳),反应的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
故答案为:(1)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(2)保持洁净与干燥(合理即可).
(3)Cl2;+1价;(4)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
点评 本题难度不大,掌握工业上炼铁的反应原理、防止铁制品生锈的原理(隔绝氧气和水)与措施、化合价的计算、化学方程式的书写等是正确解答本题的关键.

| 物质 | 苯 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 3.9 | 9.6 | 0 | 0 | 0 |
| 反应中质量/g | 2.6 | 6.4 | 2.2 | 0.9 | m |
| 反应后质量/g | a | b | c | 2.7 | n |
| A. | 表中m=1.4,n=3.2 | B. | 该反应属于置换反应 | ||
| C. | 物质X中一定没有碳元素 | D. | 物质X中一定没有氢元素 |
| 反应时间/s | t1 | t2 | t3 | t4 | t5 |
| 生成H2的总质量/g | 0.03 | 0.06 | 0.08 | 0.10 | 0.10 |
(2)计算黄铜样品中铜的质量分数.
 兴趣小组欲测试定某未知浓度Ba(OH)2溶液的溶质质量分数,请你和他们一起完成实验并回答有关问题.
兴趣小组欲测试定某未知浓度Ba(OH)2溶液的溶质质量分数,请你和他们一起完成实验并回答有关问题.