题目内容
8. 水是一种重要的资源.
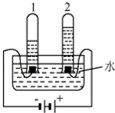
水是一种重要的资源.(1)电解水实验揭示了水的组成.如图实验中得到氧气的试管是2(填“1”或“2”),试管1和试管2中收集到的气体的体积比约等于2:1.此反应的符号表达式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;此实验说明水是由氢、氧元素组成.
(2)某同学在完成电解水实验时,发现正极产生了5mL气体,则负极产生的气体体积是10mL.
(3)自来水厂净水过程中用到活性炭,其作用是吸附.
(4)在制取蒸馏水的过程中,在水中要放碎瓷片,其作用是加热时出现暴沸.
分析 (1)在做电解水的实验时,为了增强水的导电性,可在水中加入少量稀硫酸或氢氧化钠溶液;闭合电路后,会看到试管内的电极上出现气泡,过一段时间,与电源正极相连的试管产生的气体能使带火星的木条复燃,而与电池负极相连的试管产生的气体可以燃烧,它们体积比约为1:2,由此结合化学反应的实质可以判断出水的组成.
(2)根据正极产生的是氧气,负极产生的是氢气,氧气和氢气的体积比约为1:2解答;
(3)根据活性炭具有吸附性解答;
(4)根据在制取蒸馏水的过程中,在水中要放碎瓷片,其作用是加热时出现暴沸解答.
解答 解:(1)在做电解水的实验时,为了增强水的导电性,可在水中加入少量稀硫酸或氢氧化钠溶液;闭合电路后,会看到试管内的电极上出现气泡,过一段时间,与电源正极相连的试管产生的气体能使带火星的木条复燃,为氧气,而与电池负极相连的试管产生的气体可以燃烧,为氢气,它们体积比约为1:2,即图中1中产生的气体为氢气,而2试管产生的气体为氧气,1与2中气体的体积之比为2:1;根据化学反应的实质可以知道,反应前后元素的种类不变,所以可以判断水是由氢元素和氧元素组成的.水电解的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(2)若在正极收集到10mL气体,则在负极同时可收集到20mL氢气;
(3)活性炭具有吸附性,可以吸附色素和杂质,自来水厂净水过程中用到活性炭,其作用是吸附;
(4)在制取蒸馏水的过程中,在水中要放碎瓷片,其作用是加热时出现暴沸.
答案:
(1)2; 2:1; 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;氢、氧;
(2)10;
(3)吸附;
(4)加热时出现暴沸.
点评 通过电解水的实验,可以证明水由H、O元素组成,根据电解生成氢气、氧气体积比2:1,可推导水分子中氢、氧原子个数比为2:1.

 53随堂测系列答案
53随堂测系列答案| A. | 20℃,1L水与1L酒精混合后的体积等于2L | |
| B. | 20℃,1g镁在1g氧气充分燃烧后,生成氧化镁2g | |
| C. | 20℃,1个氢分子与1个氧分子结合生成2个水分子 | |
| D. | 20℃,1g硫粉在1g氧气中完全燃烧后生成2g二氧化硫 |
| A. | 纯铁是一种黑色有光泽的金属 | |
| B. | 铁易与水反应生成铁锈 | |
| C. | 铁在常温下易与氧气反应生成四氧化三铁 | |
| D. | 铁在盐酸溶液和硫酸铜溶液中发生置换反应后,都生成+2价铁的化合物 |
| A. | 实验室常用蒸馏降低水的硬度 | B. | 通过活性炭吸附降低水的硬度 | ||
| C. | 工业废水需处理达标后排放 | D. | 水是由氢元素和氧元素组成的 |
 在点燃条件下,甲和乙反应生成丙和丁,反应前后分子变化的微观示意图如图,下列说法不正确的
在点燃条件下,甲和乙反应生成丙和丁,反应前后分子变化的微观示意图如图,下列说法不正确的是( )
| A. | 丁是人体中含量最多的物质 | |
| B. | 该反应的基本类型不是化合反应 | |
| C. | 甲和乙反应的质量比为17:32 | |
| D. | 生成物丙和丁两种物质的分子个数比为1:3 |
| A. | 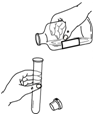 倾倒液体 | B. | 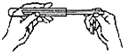 取粉末状固体药品 | ||
| C. | 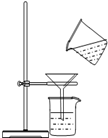 过滤 | D. | 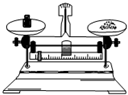 用天平称量药品 |