题目内容
如图是实验室制取气体的一些装置,据图回答有关问题.
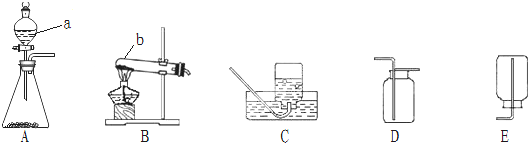
(1)写出图中有标号氧气的名称:a: b: ;
(2)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是 (填装置的字母标号),该反应的化学方程式为: ,其中二氧化锰起 作用.
(3)用C装置收集氧气的依据是 .
(4)某同学在观察到锥形瓶内有大量气泡时,开始用如图所示的D装置收集氧气,过一段时间后,用带火星的木条伸入瓶口,瓶中、瓶底,都未见木条复燃.可能的原因是 .
(5)若装置A中反应很剧烈,据此提出实验的安全注意事项是 .
A.控制液体滴加速度 B.用体积较小的锥形瓶 C.加热反应物.

(1)写出图中有标号氧气的名称:a:
(2)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是
(3)用C装置收集氧气的依据是
(4)某同学在观察到锥形瓶内有大量气泡时,开始用如图所示的D装置收集氧气,过一段时间后,用带火星的木条伸入瓶口,瓶中、瓶底,都未见木条复燃.可能的原因是
(5)若装置A中反应很剧烈,据此提出实验的安全注意事项是
A.控制液体滴加速度 B.用体积较小的锥形瓶 C.加热反应物.
考点:氧气的制取装置,氧气的收集方法,催化剂的特点与催化作用,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)认识常见仪器的名称;
(2)根据反应原理来书写化学方程式;分析二氧化锰在过氧化氢分解过程中所起的作用,用过氧化氢和二氧化锰制氧气,就不需要加热;
(3)根据氧气的性质来选择收集方法;
(4)发生装置漏气,集气瓶破损都能够导致收集的氧气不纯或收集不到氧气.
(5)可通过控制液体滴加速度来减慢化学反应速率.
(2)根据反应原理来书写化学方程式;分析二氧化锰在过氧化氢分解过程中所起的作用,用过氧化氢和二氧化锰制氧气,就不需要加热;
(3)根据氧气的性质来选择收集方法;
(4)发生装置漏气,集气瓶破损都能够导致收集的氧气不纯或收集不到氧气.
(5)可通过控制液体滴加速度来减慢化学反应速率.
解答:解:(1)①是分液漏斗;②是试管;
(2)用过氧化氢和二氧化锰制氧气,就不需要加热,故选A;过氧化氢在二氧化锰的催化作用下分解为水和氧气;
(3)因为氧气不易溶于水也不与水反应,故可用排水法来收集;
(4)发生装置漏气,集气瓶破损时,收集的氧气不纯或收集不到氧气,用带火星的木条伸入瓶口、瓶中、瓶底时,带火星的木条不能复燃.
(5)可通过控制液体滴加速度来减慢化学反应速率,故选A.
故填:故答案为:(1)分液漏斗;试管;
(2)A;2H2O2
2H2O+O2↑;催化;(3)氧气不易溶于水也不与水反应;
(4)发生装置漏气或集气瓶破损.(5)A.
(2)用过氧化氢和二氧化锰制氧气,就不需要加热,故选A;过氧化氢在二氧化锰的催化作用下分解为水和氧气;
(3)因为氧气不易溶于水也不与水反应,故可用排水法来收集;
(4)发生装置漏气,集气瓶破损时,收集的氧气不纯或收集不到氧气,用带火星的木条伸入瓶口、瓶中、瓶底时,带火星的木条不能复燃.
(5)可通过控制液体滴加速度来减慢化学反应速率,故选A.
故填:故答案为:(1)分液漏斗;试管;
(2)A;2H2O2
| ||
(4)发生装置漏气或集气瓶破损.(5)A.
点评:实验室常用玻璃仪器要准确认识,实验室制取氧气的三种方法需熟练掌握,收集气体的方法有三种:向上排空气法、向下排空气法及排水法,每种方法的适用范围要明确.

练习册系列答案
相关题目
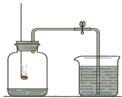 如图是测定空气中氧气体积分数的实验,实验后发现测定氧气的含量与事实有明显偏差.下列分析或做法不正确的是( )
如图是测定空气中氧气体积分数的实验,实验后发现测定氧气的含量与事实有明显偏差.下列分析或做法不正确的是( )| A、实验装置气密性不好,存在漏气的情况 |
| B、实验中点燃红磷伸入集气瓶前没有夹紧弹簧夹 |
| C、实验中可能未冷却到室温就打开弹簧夹 |
| D、将红磷换成硫粉重新实验,做对比实验进行分析 |
下列有关溶液(固体溶质)的叙述,正确的是( )
| A、某物质的饱和溶液变为不饱和溶液,溶质的质量分数一定变小 |
| B、在一定温度下,同一物质的饱和溶液一定比不饱和溶液溶质的质量分数大 |
| C、任何物质的饱和溶液,当温度降低时一定会析出溶质晶体 |
| D、饱和溶液析出晶体后,剩余溶液中溶质的质量分数一定变小 |
明向试管中加入一种药品时,先把试管倾斜,把放有药品的药匙小心运送到试管底部,再把试管直立.试管中装入的药品是( )
| A、大理石块 | B、过氧化氢 |
| C、高锰酸钾 | D、锌粒 |