题目内容
纳米级Cu2O因具有优良的催化性能备受关注.某兴趣小组同学在《培养中学生基本科学素养的化学实验教学研究》课题组老师的带领下开展了系列研究.
Ⅰ纳米级Cu2O的用途研究

【查阅资料】
①氨气是一种有刺激性气味的气体,在高浓度氧气中才能燃烧,生成氮气和水.
②在纳米级Cu2O的催化作用下,氨气与氧气在一定温度下发生以下化学反应:
4NH3+5O2═4NO+6H2O 4NH3+3O2═2N2+6H2O
工业上用NO制备硝酸、氮肥等化工产品.
【实验1】
设计图1的实验装置验证氨气在氧气中燃烧:将过量的氧气与氨气分别从a、b两管进气口通入,并在b管上端点燃氨气.实验组需先通入氧气,后通入氨气,理由是 .
【实验2】设计如图2实验装置,并对生成物进行成分分析
根据气体成分分析数据,同学们绘制了曲线图(见图3),发现在纳米级
Cu2O的催化作用下,300℃时以生产 为主.若利用后续处理装置
模拟硝酸的工业制法,最好将电热丝的温度控制在 ℃左右.
Ⅱ纳米级Cu2O的制备研究
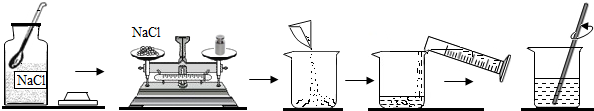
利用某些特殊的细菌,在一定条件下将某岩石中的不溶性硫化铜(CuS)转化为可溶性硫化铜,进而制得纳米级Cu2O,其流程如图4:
(1)在细菌作用下,岩石中的硫化铜(CuS)与空气中的氧气反应生成硫酸铜,反应的化学方程式为 .
(2)③中观察到的现象是 .
(3)在加热条件下,用液态肼(N2H4)还原新制Cu(OH)2生成Cu2O、N2和H2O,反应的化学方程式为 ,Cu2O中铜元素的化合价是 .
(4)经测定该岩石由硫化铜(CuS)和其他不含铜元素的物质组成.现用1000g该岩石制得21.6g纯氧化亚铜(Cu2O),该纯氧化亚铜(Cu2O)中铜元素的质量是 g.若制得氧化亚铜(Cu2O)的过程中,铜元素的总损耗为25%,通过计算确定该岩石中硫化铜(CuS)的质量分数(请写出计算过程).
Ⅰ纳米级Cu2O的用途研究

【查阅资料】
①氨气是一种有刺激性气味的气体,在高浓度氧气中才能燃烧,生成氮气和水.
②在纳米级Cu2O的催化作用下,氨气与氧气在一定温度下发生以下化学反应:
4NH3+5O2═4NO+6H2O 4NH3+3O2═2N2+6H2O
工业上用NO制备硝酸、氮肥等化工产品.
【实验1】
设计图1的实验装置验证氨气在氧气中燃烧:将过量的氧气与氨气分别从a、b两管进气口通入,并在b管上端点燃氨气.实验组需先通入氧气,后通入氨气,理由是
【实验2】设计如图2实验装置,并对生成物进行成分分析
根据气体成分分析数据,同学们绘制了曲线图(见图3),发现在纳米级
Cu2O的催化作用下,300℃时以生产
模拟硝酸的工业制法,最好将电热丝的温度控制在
Ⅱ纳米级Cu2O的制备研究
利用某些特殊的细菌,在一定条件下将某岩石中的不溶性硫化铜(CuS)转化为可溶性硫化铜,进而制得纳米级Cu2O,其流程如图4:
(1)在细菌作用下,岩石中的硫化铜(CuS)与空气中的氧气反应生成硫酸铜,反应的化学方程式为
(2)③中观察到的现象是
(3)在加热条件下,用液态肼(N2H4)还原新制Cu(OH)2生成Cu2O、N2和H2O,反应的化学方程式为
(4)经测定该岩石由硫化铜(CuS)和其他不含铜元素的物质组成.现用1000g该岩石制得21.6g纯氧化亚铜(Cu2O),该纯氧化亚铜(Cu2O)中铜元素的质量是
考点:物质的相互转化和制备,实验探究物质的组成成分以及含量,有关元素化合价的计算,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:物质的制备,有关化学方程式的计算,科学探究
分析:【实验1】根据实验目的分析;
【实验2】根据图象数据分析;
(1)根据书写方程式原则书写;
(2)根据反应物生成物分析实验现象;
(3)根据反应物生成物及写方程式原则书写;
(4)根据氧化亚铜的化学式可 求出铜元素的质量,根据元素质量守恒可求出CuS中铜元素的质量,从而求出CuS的质量与质量分数.
【实验2】根据图象数据分析;
(1)根据书写方程式原则书写;
(2)根据反应物生成物分析实验现象;
(3)根据反应物生成物及写方程式原则书写;
(4)根据氧化亚铜的化学式可 求出铜元素的质量,根据元素质量守恒可求出CuS中铜元素的质量,从而求出CuS的质量与质量分数.
解答:解:【实验1】NH3的燃烧需要高浓度氧气,先通氧气可以保证氨气被点燃.
【实验2】由图曲线可以看出,在300℃时氮气比NO产量高,以氮气为主.若利用后续处理装置模拟硝酸的工业制法,生成物中应以NO为主,因此最好将电热丝的温度控制在900℃左右.
(1)反应物是硫化铜(CuS)与空气中的氧气,生成物是硫酸铜,反应条件是细菌,化学方程式为CuS+2O2
CuSO4;
(2)③中反应是硫酸铜溶液中加入氢氧化钠,生成物中有氢氧化铜,因此可观察到产生蓝色沉淀;
(3)反应物是液态肼(N2H4)和Cu(OH)2;生成物是Cu2O、N2和H2O,反应的化学方程式为N2H4+4Cu(OH)2
2Cu2O+N2↑+6H2O,Cu2O中氧元素为-2价,根据化合物中正负化合价代数和为0可知铜元素化合价为+1价;
(4)Cu2O中铜元素质量为21.6g×
=19.2g;制得氧化亚铜(Cu2O)的过程中,铜元素的总损耗为25%,所以CuS中铜元素质量为
=25.6g,因此CuS的质量为
=38.4g,故该岩石中CuS的质量分数为
×100%=3.84%.
故答案为:【实验1】NH3的燃烧需要高浓度氧气,先通氧气可以保证氨气被点燃.
【实验2】氮气;900;
(1)CuS+2O2
CuSO4;
(2)产生蓝色沉淀;
(3)N2H4+4Cu(OH)2
2Cu2O+N2↑+6H2O;+1;
(4)19.2;3.84%.
【实验2】由图曲线可以看出,在300℃时氮气比NO产量高,以氮气为主.若利用后续处理装置模拟硝酸的工业制法,生成物中应以NO为主,因此最好将电热丝的温度控制在900℃左右.
(1)反应物是硫化铜(CuS)与空气中的氧气,生成物是硫酸铜,反应条件是细菌,化学方程式为CuS+2O2
| ||
(2)③中反应是硫酸铜溶液中加入氢氧化钠,生成物中有氢氧化铜,因此可观察到产生蓝色沉淀;
(3)反应物是液态肼(N2H4)和Cu(OH)2;生成物是Cu2O、N2和H2O,反应的化学方程式为N2H4+4Cu(OH)2
| ||
(4)Cu2O中铜元素质量为21.6g×
| 128 |
| 144 |
| 19.2g |
| 1-25% |
| 25.6g | ||
|
| 38.4g |
| 1000g |
故答案为:【实验1】NH3的燃烧需要高浓度氧气,先通氧气可以保证氨气被点燃.
【实验2】氮气;900;
(1)CuS+2O2
| ||
(2)产生蓝色沉淀;
(3)N2H4+4Cu(OH)2
| ||
(4)19.2;3.84%.
点评:本题是一道实验信息题,阅读量较大,但题目设计不难,关键是细心耐心的读完题意才能较好答题.

练习册系列答案
相关题目