题目内容
黄铜是由铜、锌组成的合金.为测定某种黄铜中锌的含量,取43.4g这种黄铜和质量分数为19.6%的硫酸溶液100g恰好完全反应,将未反应的铜过滤后得到112.6g溶液.
试计算(计算结果保留1位小数)
(1)合金中锌的质量分数;
(2)反应后所得 溶液中溶质的质量分数.
溶液中溶质的质量分数.
| (1)根据反应消耗的稀硫酸的质量,然后利用锌与硫酸反应的化学方程式,求出锌的质量即可; (2)反应后所得溶液中溶质为硫酸锌,可根据硫酸中溶质的质量求出硫酸锌的质量,进而根据溶质的质量分数的计算公式完成解答即可.. | |
| 解答: | 解:(1)由题意可以知道反应消耗的硫酸中溶质的质量为:100g×19.6%=19.6g. 设合金中锌的质量为x,硫酸锌的质量为y. Zn+H2SO4═ZnSO4+H2↑ 65 98 161 x 19.6g y
解得:x=13g y=32.2g 所以合金中锌的质量分数为: (2)反应后所得溶液中溶质的质量分数为: 答:(1)合金中锌的质量分数为30%; (2)反应后所得溶液中溶质的质量分数为28.6%. |

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
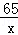 =
=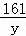 =
=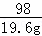
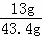 ×100%=30%
×100%=30%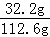 ×100%=28.6%
×100%=28.6%