题目内容
15.化学实验小组的同学为确定某石灰石中碳酸钙的质量分数,进行了如表所示的实验:| 实验编号 | 石灰石的质量/g | 加入稀盐酸的质量/g | 剩余固体质量/g |
| 实验1 | 20 | 40 | 8.0 |
| 实验2 | 20 | 60 | 3.5 |
| 实验3 | 20 | 80 | 3.5 |
(2)计算实验中所用稀盐酸的溶质质量分数.
分析 首先正确写出方程式,然后根据题干内容分析得出反应后剩余固体即为杂质,质量差即为碳酸钙的质量结合化学方程式可以计算所用稀盐酸的溶质质量,就可以进一步求出所用稀盐酸的溶质质量分数.
解答 解:(1)石灰石中碳酸钙的质量是20g-3.5g=16.5g;
该石灰石中碳酸钙的质量分数为$\frac{16.5g}{20g}$×100%=82.5%;
(2)当加入稀盐酸的质量为40g时,剩余固体质量为8.0g,说明盐酸完全反应.
设40g稀盐酸的溶质质量为x,
CaCO3 +2HCl=CaCl2 +H2O+CO2↑
100 73
20g-8g x
$\frac{100}{20g-8g}=\frac{73}{x}$
x=8.76g
实验中所用稀盐酸的溶质质量分数=$\frac{8.76g}{40g}$×100%=21.9%
答案:
(1)82.5%;
(2)实验中所用稀盐酸的溶质质量分数为21.9%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.水是生命之源,也是重要的溶剂,下列有关水的说法正确的是( )
| A. | 长期饮用蒸馏水有益身体健康 | |
| B. | 水电解生成氢气和氧气,说明水中含有氢分子和氧分子 | |
| C. | 将湘江水经过沉降、过滤、吸附、灭菌等净化操作后,可供人们生活用水 | |
| D. | 水体有一定的自净功能,造纸厂的污水可直接排放到湘江 |
3.下列措施中,不宜用于博物馆保存枪支大炮等铁质文物的是( )
| A. | 定期用湿布擦拭铁制文物 | B. | 提醒游客不要用手触摸文物 | ||
| C. | 保持展室内空气的干燥 | D. | 在铁制文物表面添加保护 |
10.利用分子知识对下列现象的解释合理的是( )
| A. | 气体更易被压缩--构成气体的分子具有弹性 | |
| B. | 液氧为淡蓝色--氧气分子是蓝色的 | |
| C. | 湿衣服变干--水分子在不断地运动 | |
| D. | 碘受热升华--碘分子变大了 |
20.下列对知识的归纳和整理正确的是( )
| A. | 浓盐酸在空气中防止一段时间后质量减少,是由于盐酸易分解 | |
| B. | 一氧化碳和二氧化碳的性质存在差异,是由于他们的组成元素不同 | |
| C. | 酸具有相似的化学性质,是由于酸溶液中都含有氢离子 | |
| D. | 水结冰后化学性质没有发生变化,是由于水分子之间的间隔没有发生变化 |
7.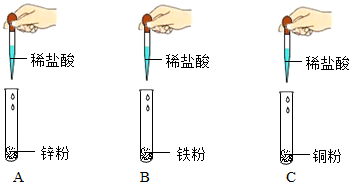 某化学兴趣小组的同学在探究“酸的化学性质”时,做了如图实验.写出实验中的一个化学方程式Fe+2HCl═FeCl2+H2↑.实验结束后,同学们将三支试管中的药品同时倒入同一个洁净的烧杯中,观察到固体表面有气泡冒出,直至不再产生气泡时发现烧杯底部有一些固体,上层为浅绿色的溶液.兴趣小组的同学对上层清液中的溶质成分展开了如下探究.
某化学兴趣小组的同学在探究“酸的化学性质”时,做了如图实验.写出实验中的一个化学方程式Fe+2HCl═FeCl2+H2↑.实验结束后,同学们将三支试管中的药品同时倒入同一个洁净的烧杯中,观察到固体表面有气泡冒出,直至不再产生气泡时发现烧杯底部有一些固体,上层为浅绿色的溶液.兴趣小组的同学对上层清液中的溶质成分展开了如下探究.
【提出问题】溶液中的溶质有哪些呢?
【做出猜想】猜想一:溶质是氯化锌、氯化亚铁;
猜想二:溶质是氯化锌、氯化亚铁、氯化铜;
猜想三:溶质是氯化锌、氯化亚铁、氯化氢.
乐乐同学认为上述有一个猜想不合理,请你指出不合理的猜想,并说明理由猜想二;铜在氢的后面,与酸不反应,不会生成氯化铜.
【进行实验】同学们设计了如下实验验证了其它两种假设.
【实验总结】通过以上探究同学们认为烧杯底部的固体物质是Cu.(写化学用语)
 某化学兴趣小组的同学在探究“酸的化学性质”时,做了如图实验.写出实验中的一个化学方程式Fe+2HCl═FeCl2+H2↑.实验结束后,同学们将三支试管中的药品同时倒入同一个洁净的烧杯中,观察到固体表面有气泡冒出,直至不再产生气泡时发现烧杯底部有一些固体,上层为浅绿色的溶液.兴趣小组的同学对上层清液中的溶质成分展开了如下探究.
某化学兴趣小组的同学在探究“酸的化学性质”时,做了如图实验.写出实验中的一个化学方程式Fe+2HCl═FeCl2+H2↑.实验结束后,同学们将三支试管中的药品同时倒入同一个洁净的烧杯中,观察到固体表面有气泡冒出,直至不再产生气泡时发现烧杯底部有一些固体,上层为浅绿色的溶液.兴趣小组的同学对上层清液中的溶质成分展开了如下探究.【提出问题】溶液中的溶质有哪些呢?
【做出猜想】猜想一:溶质是氯化锌、氯化亚铁;
猜想二:溶质是氯化锌、氯化亚铁、氯化铜;
猜想三:溶质是氯化锌、氯化亚铁、氯化氢.
乐乐同学认为上述有一个猜想不合理,请你指出不合理的猜想,并说明理由猜想二;铜在氢的后面,与酸不反应,不会生成氯化铜.
【进行实验】同学们设计了如下实验验证了其它两种假设.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,向取中滴加紫色石蕊试液 | 溶液变为红色 | 猜想三正确 |
4.“饮食健康“是人们普遍的生活追求,下列做法正确的是( )
| A. | 用甲醛水溶液浸泡海产品,以防其腐烂 | |
| B. | 在炒熟的菜中放入适量的加碘食盐,使其美味 | |
| C. | 在果汁中加入“塑化剂”,使其口感更好 | |
| D. | 在火腿肠中添加工业用盐亚硝酸钠,使其保持肉质鲜美 |