题目内容
如图装置测定因存放不当而部分变成碳酸钠的烧碱中氢氧化钠的质量分数.所取试样质量8.00g、锥形瓶质量140.00g,加入足量稀硫酸(质量为50.00g)每隔相同时间读数一次,数据如下表:(1)不必进行第七次读数的原因是______;
(2)计算试样中氢氧化钠的质量分数.(写出具体的计算过程)
| 读数次数 | 质量/g | |
| 锥形瓶+试样+稀硫酸 | 第1次 | 197.64 |
| 第2次 | 197.48 | |
| 第3次 | 197.26 | |
| 第4次 | 197.16 | |
| 第5次 | 197.12 | |
| 第6次 | 197.12 |

【答案】分析:根据固体混合物与硫酸的反应,分析所记录的数据,利用质量守恒定律,装置减少的质量就是反应放出二氧化碳的质量;
结合反应的化学方程式,由二氧化碳气体的质量计算出参加反应的碳酸钠的质量,从而求出氢氧化钠的质量及质量分数.
解答:解:(1)第5次和第6次读数均为197.12,读数相同,总质量不再改变,说明此时不再放出气体,反应已经结束;
故答案为:第5次和第6次读数相同,已充分反应;
(2)根据质量守恒定律,CO2的质量是:(8.00 g+140.00 g+50.00 g)-197.12 g=0.88 g
设样品中Na2CO3的质量为x.
Na2CO3+H2SO4═H2O+CO2↑+Na2SO4
106 44
x 0.88 g
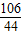 =
=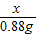
解之得 x=2.12 g
则所取样品中NaOH的质量分数为: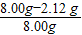 ×100%=73.5%
×100%=73.5%
答:试样中氢氧化钠的质量分数为73.5%.
点评:本题考查了学生分析数据解答问题的能力,解题时注意分析所给数据中的相同数据再结合所发生的化学反应仔细分析,即可找出已知量进一步分析解答.
结合反应的化学方程式,由二氧化碳气体的质量计算出参加反应的碳酸钠的质量,从而求出氢氧化钠的质量及质量分数.
解答:解:(1)第5次和第6次读数均为197.12,读数相同,总质量不再改变,说明此时不再放出气体,反应已经结束;
故答案为:第5次和第6次读数相同,已充分反应;
(2)根据质量守恒定律,CO2的质量是:(8.00 g+140.00 g+50.00 g)-197.12 g=0.88 g
设样品中Na2CO3的质量为x.
Na2CO3+H2SO4═H2O+CO2↑+Na2SO4
106 44
x 0.88 g
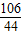 =
=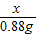
解之得 x=2.12 g
则所取样品中NaOH的质量分数为:
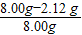 ×100%=73.5%
×100%=73.5%答:试样中氢氧化钠的质量分数为73.5%.
点评:本题考查了学生分析数据解答问题的能力,解题时注意分析所给数据中的相同数据再结合所发生的化学反应仔细分析,即可找出已知量进一步分析解答.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
