题目内容
7.在天平两端的托盘上各放质量相同的两只小烧杯,左盘烧杯中盛放过氧化氢溶液,右盘放等质量的水,天平平衡.现向两个烧杯中分别加入等质量的二氧化锰,反应过程中天平的指针向右(填“左”或“右”或“不变”)倾斜.分析 两烧杯中加入二氧化锰后;过氧化氢溶液在二氧化锰的作用下迅速分解放出氧气,从而使左盘溶液质量减少;而水在加入二氧化锰后不会分解,因此质量不会变化,由此分析.
解答 解:根据题意,两烧杯中加入二氧化锰后;过氧化氢溶液在二氧化锰的作用下迅速分解放出氧气,从而使左盘溶液质量减少;而水在加入二氧化锰后不会分解,因此质量不会变化,则托盘天平左边因放出氧气造成质量小于右边,所以,天平指针向右偏转.
故填.右
点评 天平指针会偏向质量较大的一边,因此,对比反应是否放出气体是解答此问题的核心.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
18. 同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行了探究.
同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行了探究.
【推理假设】上述两种反应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑.由此推测出废液中一定有NaCl,可能有Na2CO3或盐酸.
【实验探究】
(一)确定废液中是否含有盐酸
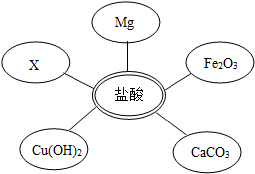
(1)选择试剂:根据盐酸的化学性质,同学们选用了如图所示的五种物质,其中物质X是酸碱指示剂中的石蕊溶液.
(2)实验验证:某同学向废液中加入少量的镁粉,观察到不产生气泡,确定废液中一定没有盐酸.
(二)确定废液中是否含有Na2CO3某同学选用pH试纸测出废液的pH=10,确定废液中一定含有Na2CO3
(三)处理废液,回收利用
欲从废液中得到纯净的NaCl,设计了如下实验方案,请完成方案评价.
 同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行了探究.
同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行了探究.【推理假设】上述两种反应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑.由此推测出废液中一定有NaCl,可能有Na2CO3或盐酸.
【实验探究】
(一)确定废液中是否含有盐酸
(1)选择试剂:根据盐酸的化学性质,同学们选用了如图所示的五种物质,其中物质X是酸碱指示剂中的石蕊溶液.
(2)实验验证:某同学向废液中加入少量的镁粉,观察到不产生气泡,确定废液中一定没有盐酸.
(二)确定废液中是否含有Na2CO3某同学选用pH试纸测出废液的pH=10,确定废液中一定含有Na2CO3
(三)处理废液,回收利用
欲从废液中得到纯净的NaCl,设计了如下实验方案,请完成方案评价.
| 方案 | 加入试剂 | 分离方法 | 方案评价 |
| 一 | 适量的Ca(NO3)2溶液 | 过滤、蒸发结晶 | 不可行(选填“可行”或“不可行”,下同) |
| 二 | 适量的稀盐酸 | 蒸发结晶 | 可行 |
12.下面是五种粒子的结构示意图,由此你能得到的正确信息是( )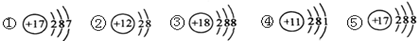
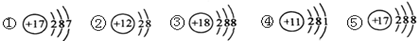
| A. | 它们表示五种元素 | |
| B. | ②③⑤三种粒子表示具有相对稳定结构的原子 | |
| C. | 其中有两种表示原子结构示意图 | |
| D. | ②表示的粒子可以用Mg2+表示 |
16.2014年9月29日中午,日本中部火山御岳山突然喷发.由于正值登山旺季,数百名游客受困山上,伤亡惨重.火山喷发时释放出大量的SO2气体.下列关于SO2的说法中不正确的是( )
| A. | SO2 是形成酸雨的一种气体 | |
| B. | SO2的相对分子质量为64 g | |
| C. | SO2中硫元素和氧元素的质量比为1:1 | |
| D. | SO2中硫元素的质量分数为50% |
8.关于水的叙述下列说法不正确的是( )
| A. | 水是由氢元素和氧元素组成的 | |
| B. | 一个水分子是由2个氢原子和1个氧原子构成的 | |
| C. | 水分子中有3个原子核 | |
| D. | 水分子中氢、氧原子个数比为2:1 |
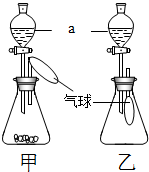 某化学兴趣小组设计了一组“吹气球”实验,两套装置如图所示:
某化学兴趣小组设计了一组“吹气球”实验,两套装置如图所示: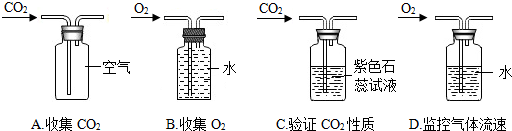

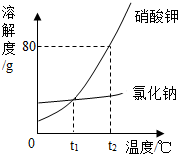 如图是氯化钠与硝酸钾的溶解度曲线,回答下列问题.
如图是氯化钠与硝酸钾的溶解度曲线,回答下列问题.