题目内容
5.化学课外活动中,小红将稀盐酸加入盛有澄清石灰水的试管中,无明显现象;小强将稀盐酸加入盛有K2CO3溶液的试管中,有气体生成.反应结束后,两同学把废液倒入同一废液缸中,观察到废液缸中产生少量的气泡,最终有白色沉淀生成.请回答以下问题:(1)废液缸中最终生成的白色沉淀是CaCO3.
(2)通过分析废液缸中的现象,你认为小红实验后的废液中一定含有的物质是CaCl2和HCl.
(3)小强从废液缸中取出废液,过滤,对滤液进行实验探究.他认为滤液中除含有KCl外,还可能含有K2CO3,请你邦他完成下面的实验报告:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,加入 稀盐酸 | 有气泡产生 | 滤液中含有K2CO3 |
K2CO3+2HCl═2KCl+H2O+CO2↑、CaCl2+K2CO3═CaCO3↓+2KCl.
分析 (1)“稀盐酸与澄清石灰水反应”,生成氯化钙;“将稀盐酸加入盛有K2CO3溶液的试管中”,有气体和氯化钾生成;“观察到废液缸中产生少量的气泡,最终有白色沉淀生成”,则白色沉淀为碳酸钙;
(2)因为“观察到废液缸中产生少量的气泡”,则一定有盐酸;“最终有白色沉淀生成”一定含有钙离子;
(3)“将稀盐酸加入盛有K2CO3溶液的试管中”,有气体和氯化钾生成;“观察到废液缸中产生少量的气泡,最终有白色沉淀生成”,则还可能含有K2CO3;验证碳酸钾,用酸或钙盐、钡盐及其它对应的碱溶液等,合理即可.
(4)根据反应物和生成物书写反应的化学方程式即可.
解答 解:(1)氯化钙与碳酸钾反应,生成碳酸钙,其化学式为CaCO3;
(2)由分析可知“观察到废液缸中产生少量的气泡,最终有白色沉淀生成”,因为“观察到废液缸中产生少量的气泡”,则一定有盐酸;“最终有白色沉淀生成”一定含有钙离子;则小红实验后的废液中一定含有的物质是CaCl2和HCl;
(3)“将稀盐酸加入盛有K2CO3溶液的试管中”,有气体和氯化钾生成;“观察到废液缸中产生少量的气泡,最终有白色沉淀生成”,则还可能含有K2CO3;验证碳酸钾,用酸或钙盐、钡盐及其它对应的碱溶液等,现象必须与选取试剂相对应.故
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,加入稀盐酸 | 有气泡产生 | 滤液中含有K2CO3. |
故答案为:(1)CaCO3;
(2)CaCl2和HCl;
(3)
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,加入 稀盐酸 | 有气泡产生 | 滤液中含有K2CO3. |
(4)K2CO3+2HCl═2KCl+H2O+CO2↑,CaCl2+K2CO3═CaCO3↓+2KCl.
点评 本题考查的是酸碱盐之间反应剩余物成分的确定,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
相关题目
16.下列物质的用途叙述不正确的是( )
| A. | 氢氧化钠用来治疗胃酸过多 | |
| B. | 服用鸡蛋清可以缓解重金属盐中毒 | |
| C. | 生石灰可以用作食品包装袋中的干燥剂 | |
| D. | 铵态氮肥不能和碱性物质混用 |
17.以下四个实验的设计,其中不合理的是( )
| 选项 | A | B | C | D |
| 目的 | 区分食盐水和稀盐酸 | 区分羊毛绒和棉线 | 区分硝酸铵粉末和氧化钙粉末 | 区分聚乙烯和聚氯乙烯 |
| 方案 | 滴加硝酸银溶液 | 灼烧闻气味 | 加水 | 灼烧闻气味 |
| A. | A | B. | B | C. | C | D. | D |
14.下列做法错误的是( )
| A. | 食用瘦肉等含铁食物预防缺铁性贫血 | |
| B. | 用聚氯乙烯塑料制成食品保鲜膜 | |
| C. | 碳酸氢钠和柠檬酸、水等混合可制成汽水 | |
| D. | 用汽油或水均能很容易地鉴别出高锰酸钾和碘两种暗紫色固体 |
15.世界是物质的,物质是变化的.下列变化属于化学变化的是( )
| A. | 水结成冰 | B. | 葡萄酿酒 | C. | 矿石粉碎 | D. | 酒精挥发 |
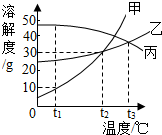 甲乙丙三种固体物质的溶解度曲线如图所示,回答下列问题.
甲乙丙三种固体物质的溶解度曲线如图所示,回答下列问题.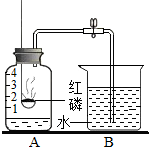 某同学用如图装置是测定空气中氧气含量的实验,先把A中水面以上分成五等份由下至上刻度分为1、2、3、4.请你填写有关空格.
某同学用如图装置是测定空气中氧气含量的实验,先把A中水面以上分成五等份由下至上刻度分为1、2、3、4.请你填写有关空格.