题目内容
14.在稀盐酸中滴加几滴酚酞溶液,然后再加入足量的下列试剂,最终溶液不可能为红色的是( )| A. | 石灰水 | B. | 稀硫酸 | C. | 氢氧化钠溶液 | D. | 石蕊溶液 |
分析 根据紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝;无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红,据此结合酸的化学性质,进行分析解答.
解答 解:A、在稀盐酸中滴加几滴酚酞溶液,然后再加入足量的石灰水,稀盐酸与石灰水发生中和反应生成氯化钙和水,最终溶液为氯化钙和石灰水的混合溶液,显碱性,最终溶液为红色,故选项错误.
B、在稀盐酸中滴加几滴酚酞溶液中加入稀硫酸,溶液为盐酸和硫酸的混合溶液,显酸性,不能使酚酞溶液变红色,故选项正确.
C、在稀盐酸中滴加几滴酚酞溶液,然后再加入足量的氢氧化钠溶液,稀盐酸与氢氧化钠溶液发生中和反应生成氯化钠和水,最终溶液为氯化钠和氢氧化钠的混合溶液,显碱性,最终溶液为红色,故选项错误.
D、在稀盐酸中滴加几滴酚酞溶液,再加入足量的石蕊溶液,紫色石蕊溶液遇酸性溶液变红,溶液变红色,故选项错误.
故选:B.
点评 本题难度不大,熟练掌握常见酸碱指示剂的性质、酸的化学性质并能灵活运用是正确解答本题的关键.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
5.下列实验现象描述不正确的是( )
| A. | 红磷在空气中燃烧,产生大量白烟 | |
| B. | 木炭在氧气中燃烧,发出白光,生成无色气体 | |
| C. | 细铁丝在氧气中燃烧,火星四射,生成黑色固体 | |
| D. | 纯净氢气在氧气中燃烧时,火焰呈黄色并放出热量 |
2.某化学兴趣小组同学用大理石和盐酸反应制取CO2,将制得的气体通人澄清石灰水时,未变浑浊,便产生了好奇.对此展开了探究活动,请你参与探究并填写空格.
提出问题:澄清石灰水未变浑浊的原因是什么?
假设猜想:假设一:石灰水变质 假设二:制得气体中无CO2
探究实验:为探究假设是否成立,小组同学取原试剂瓶中澄清石灰水进行如下实验:
写出上述实验中澄清石灰水变浑浊的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
分析推理:通过上述探究,否定了两个假设,小组同学确定澄清石灰水未变浑浊是其他原因造成的.于是他们对反应物进行了分析,根据盐酸的挥发性,推测制得气体中有较多的HCl气体.通过查阅资料得知HCl气体通入AgNO3溶液中会生成AgCl,该物质为白色,不溶于水也不溶于酸,为了验证推测,小组同学又进行了如下实验:
得出结论:澄清石灰水未变浑浊的原因是制得的CO2中有一定量HCl气体.有一定量HCl气体存在时,澄清石灰水为什么不变浑浊?请解释HCl溶于水形成盐酸,无法生成碳酸钙沉淀(可用化学方程式表示).
评价反思:小组中有一位同学认为.验证实验:中不能用紫色石蕊溶液证明HCl气体的存在,原因是二氧化碳通入紫色石蕊试液中,溶液也会变红.
拓展迁移:实验室制取气体要考虑诸多因素,如反应速率是否适中、制得气体是否纯净等.实验室制取CO2通常用大理石或石灰石和稀盐酸,而不用碳酸钠和稀盐酸,原因是反应太快不便于控制.
提出问题:澄清石灰水未变浑浊的原因是什么?
假设猜想:假设一:石灰水变质 假设二:制得气体中无CO2
探究实验:为探究假设是否成立,小组同学取原试剂瓶中澄清石灰水进行如下实验:
| 实验操作 |  |  |
| 实验现象 | 澄清石灰水变浑浊 | 试管1澄清石灰水未变浑浊 试管2澄清石灰水变浑浊 |
实验结论 | 说明石灰水未变质 | 说明制的气体中有CO2或二氧化碳气体 |
分析推理:通过上述探究,否定了两个假设,小组同学确定澄清石灰水未变浑浊是其他原因造成的.于是他们对反应物进行了分析,根据盐酸的挥发性,推测制得气体中有较多的HCl气体.通过查阅资料得知HCl气体通入AgNO3溶液中会生成AgCl,该物质为白色,不溶于水也不溶于酸,为了验证推测,小组同学又进行了如下实验:
| 实验操作 | 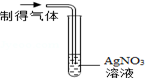 |  |
| 实验现象 | 出现白色沉淀 | 紫色石蕊溶液变红 |
| 实验结论 | 有HCl气体 | 有HCl气体 |
评价反思:小组中有一位同学认为.验证实验:中不能用紫色石蕊溶液证明HCl气体的存在,原因是二氧化碳通入紫色石蕊试液中,溶液也会变红.
拓展迁移:实验室制取气体要考虑诸多因素,如反应速率是否适中、制得气体是否纯净等.实验室制取CO2通常用大理石或石灰石和稀盐酸,而不用碳酸钠和稀盐酸,原因是反应太快不便于控制.
9.下列溶液中,既能与酸反应又能与碱反应的是( )
| A. | FeC13溶液 | B. | Na0H溶液 | C. | HCl溶液 | D. | K2CO3溶液 |
7.下列属于纯净物的是( )
| A. | 食醋 | B. | 啤酒 | C. | 加碘食盐 | D. | 冰水混合 |

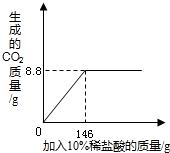 一同学在实验室测定某石灰石样品中CaCO3的质量分数(杂质不与酸反应,也不溶于水).他取了25g样品放在锥形瓶中,加入一定量的10%的稀盐酸,通过测定,反应消耗稀盐酸的质量与生成二氧化碳的质量关系如图所示.试求:
一同学在实验室测定某石灰石样品中CaCO3的质量分数(杂质不与酸反应,也不溶于水).他取了25g样品放在锥形瓶中,加入一定量的10%的稀盐酸,通过测定,反应消耗稀盐酸的质量与生成二氧化碳的质量关系如图所示.试求: 已知A、B为两种单质,甲、乙为两种化合物,且甲、乙组成元素相同,它们都是初中化学中常见的物质.它们之间的相互转化关系如图:
已知A、B为两种单质,甲、乙为两种化合物,且甲、乙组成元素相同,它们都是初中化学中常见的物质.它们之间的相互转化关系如图: 儿童缺锌会引起食欲不振、发育不良.如图为某种补锌口服液说明书的一部分,请回答:
儿童缺锌会引起食欲不振、发育不良.如图为某种补锌口服液说明书的一部分,请回答: