题目内容
2.化合物C3H8O3和化合物C7H8组成的混合物中,碳元素的质量分数为51.3%,则混合物此时氧元素含量为( )| A. | 20% | B. | 30% | C. | 40% | D. | 50% |
分析 C7H8和C3H8O3的相对分子质量相等,分子中H原子个数相等,则H的质量分数相同,两物质以任意比混合H的质量分数不变,根据化学式计算H元素质量分数,再根据w(O)=1-w(C)-w(H)计算
解答 解:C7H8和C3H8O3的相对分子质量为92,1个分子中H原子个数相等,所以两者H的质量分数为$\frac{1×8}{92}$×100%=8.7%,两物质混合后H的质量分数不变,所以混合物中H的质量分数为8.7%,混合物中碳元素的质量分数为51.3%,则混合物此时氧元素含量为1-51.3%-8.7%=40%,
故选C.
点评 本题考查混合物中元素质量分数计算,难度中等,关键是根据化学式确定所含H的质量分数,属于巧解巧算,重在考查学生的分析思维能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.“金银铜铁锡”俗称五金,是被广泛使用的金属材料.在这五种金属中,活动性最弱的是( )
| A. | 金 | B. | 银 | C. | 铁 | D. | 锡 |
14.已知Cu2O+H2SO4═CuSO4+Cu+H2O,称取5.00g铜和氧化亚铜的混合固体加入到足量稀硫酸溶液中使其充分反应后,过滤、洗涤、干燥,称量得红色固体质量为4.10g.则原来混合固体中氧化亚铜的质量分数为( )
| A. | 16.2% | B. | 32.4% | C. | 41% | D. | 82% |
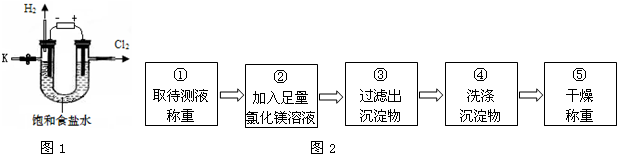
11.某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图1所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下探究.
老师提示:I.电解饱和食盐水的化学方程式:
2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑
Ⅱ.忽略其他可能发生的反应对以下实验的影响.
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,请你将实验报告填写完整.
探究活动二:测定待测液中氢氧化钠的质量分数
【实验1】用酸碱中和法测定
甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加
入一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据
如下:
(2)写出氢氧化钠与稀盐酸反应的化学方程式:NaOH+HCl═NaCl+H2O.
(3)利用氢氧化钠与稀盐酸恰好完全反应时的实验数据,计算所称取待测液中氢氧化钠的质量,应从选用稀盐酸的体积为9.8mL.
【实验2】用沉淀法测定
资料摘要:氢氧化钠与氯化镁溶液中发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl
乙组同学按图2所示的实验步骤进行实验:
(4)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取上层清液于试管中,向试管中滴加氢氧化钠溶液,产生白色沉淀,氯化镁已经过量(写出实验步骤、现象和结论).
(5)步骤③过滤出的沉淀物是氢氧化镁.
(6)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
老师提示:I.电解饱和食盐水的化学方程式:
2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑

Ⅱ.忽略其他可能发生的反应对以下实验的影响.
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,请你将实验报告填写完整.
| 实验步骤 | 实验现象 | 实验结论 |
向待测液中滴加几滴酚酞试液 | 酚酞试液变红色 | 待测液呈碱性,表明含有氢氧化钠 |
【实验1】用酸碱中和法测定
甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加
入一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据
如下:
| 加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
| 烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
(3)利用氢氧化钠与稀盐酸恰好完全反应时的实验数据,计算所称取待测液中氢氧化钠的质量,应从选用稀盐酸的体积为9.8mL.
【实验2】用沉淀法测定
资料摘要:氢氧化钠与氯化镁溶液中发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl
乙组同学按图2所示的实验步骤进行实验:
(4)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取上层清液于试管中,向试管中滴加氢氧化钠溶液,产生白色沉淀,氯化镁已经过量(写出实验步骤、现象和结论).
(5)步骤③过滤出的沉淀物是氢氧化镁.
(6)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
12.有关分离液态空气制氧气的说法正确的是( )
| A. | 利用了液氮比液氧的沸点低 | B. | 制得的氧气为纯氧 | ||
| C. | 发生的是化学变化 | D. | 贮存氧气是在黑色钢瓶中 |
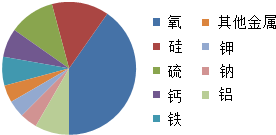 据报道:一颗陨石在俄罗斯中部乌拉尔山区坠落,陨石进入大气层时,速度达到了音速的40倍,而落地前的速度减小到了30千米/时,由此引发的“陨石雨”导致1200多名当地居民受伤.
据报道:一颗陨石在俄罗斯中部乌拉尔山区坠落,陨石进入大气层时,速度达到了音速的40倍,而落地前的速度减小到了30千米/时,由此引发的“陨石雨”导致1200多名当地居民受伤. 小红同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会后,采用如图所示装置将上层液体进行过滤,请问:
小红同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会后,采用如图所示装置将上层液体进行过滤,请问: