题目内容
10.为验证铁、铜、银三种金属的活动性强弱,不需要进行下列哪组实验( )| A. | 将打磨过的铁片放入稀盐酸中 | B. | 将打磨过的铜片放入稀盐酸中 | ||
| C. | 将打磨过的铜片放入硝酸银溶液中 | D. | 将打磨过的银片放入稀盐酸中 |
分析 根据金属活动顺序表的应用设计实验,去验证金属的活动性性强弱.氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应;前边的金属会把后边的金属从其盐溶液中置换出来.
解答 解:由金属活动顺序表的应用分析四个实验,发现验证实验的设计思路为:根据金属与盐酸反应情况,可验证铁的活动性比铜强;然后利用金属铜和硝酸银的置换结果,验证铜的活动性比银强.即可得出铁、铜、银三种金属的活动性强弱.对比四个实验,实验D证明金属银不能置换出酸中的氢,已证明了铜不能与盐酸,所以实验D不必进行.
故选:D.
点评 验证金属活动性时,若验证三种金属的活动性,可采取“三取中”的方法一次性完成验证,即取活动性处于中间的那种金属的可溶性盐进行金属和盐溶液的置换进行验证.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列说法正确的是( )
| A. | 在相同温度下,同一物质的饱和溶液与不饱和溶液所含溶质的质量一定不相等 | |
| B. | 25℃时,向一定质量的饱和澄清石灰水中加少量CaO,溶质的质量变小 | |
| C. | 25℃时,某NaCl溶液蒸发10g水,析出ag晶体,再蒸发10g水又析出bg晶体,则a一定等于b | |
| D. | 将100g质量分数为10%的NaOH溶液变成20%的NaOH溶液,可以加入10gNaOH或蒸发溶剂质量的一半 |
5.某气体由H2、CO2、CO、CH4中的两种组成,为确定其成分进行了下面的实验:
①将气体通过澄清的石灰水,未出现浑浊现象;
②将气体通过灼热的氧化铜,有红色固体生成;
③将气体点燃后通入澄清的石灰水,有浑浊现象
那么对该气体成分作出的以下推断中,合理的是( )
①H2、CO ②CO、CH4 ③CO2、CH4 ④H2、CH4 ⑤H2、CO、CH4.
①将气体通过澄清的石灰水,未出现浑浊现象;
②将气体通过灼热的氧化铜,有红色固体生成;
③将气体点燃后通入澄清的石灰水,有浑浊现象
那么对该气体成分作出的以下推断中,合理的是( )
①H2、CO ②CO、CH4 ③CO2、CH4 ④H2、CH4 ⑤H2、CO、CH4.
| A. | ①②③④⑤ | B. | ①②④⑤ | C. | ①②④ | D. | ①② |
19.下列物质的用途,主要利用其物理性质的是( )
| A. | 氧气用于炼钢 | B. | 干冰作制冷剂 | ||
| C. | 一氧化碳用于炼铁 | D. | 稀盐酸除铁锈 |

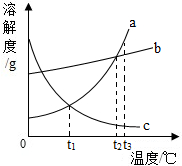 如图中a、b、c分别表示三种物质的溶解度曲线.
如图中a、b、c分别表示三种物质的溶解度曲线.