题目内容
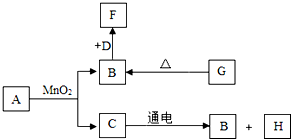
11.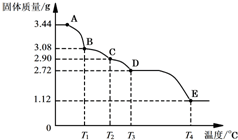 CaSO4•2H2O受热会逐步失去结晶水.取纯净的CaSO4•2H2O固体3.44g进行加热,测定固体质量随温度的变化情况如图所示.C点固体的化学式是2CaSO4•H2O.T3~T4温度段加热固体所产生的气体是形成酸雨的主要物质之一,则D~E段发生反应的化学方程式为2CaSO4$\frac{\underline{\;高温\;}}{\;}$2CaO+2SO2↑+O2↑.
CaSO4•2H2O受热会逐步失去结晶水.取纯净的CaSO4•2H2O固体3.44g进行加热,测定固体质量随温度的变化情况如图所示.C点固体的化学式是2CaSO4•H2O.T3~T4温度段加热固体所产生的气体是形成酸雨的主要物质之一,则D~E段发生反应的化学方程式为2CaSO4$\frac{\underline{\;高温\;}}{\;}$2CaO+2SO2↑+O2↑.
分析 根据生石膏在加热的条件下失去部分结晶水变成熟石膏,依据题中的数据进行计算,T3~T4温度段加热固体所产生的气体是形成酸雨的主要物质之一,所以该阶段反应生成二氧化硫气体,硫酸钙在高温的条件下生成氧化钙、二氧化硫和氧气进行分析.
解答 解:设C点固体的化学式是CaSO4•xH2O,
CaSO4•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CaSO4•xH2O+(2-x)H2O
172 136+18x
3.44g 2.90g
$\frac{172}{3.44g}$=$\frac{136+18x}{2.9g}$
x=0.5
所以C点固体的化学式是2CaSO4•H2O,
硫酸钙在高温的条件下生成氧化钙、二氧化硫和氧气,化学方程式为:2CaSO4$\frac{\underline{\;高温\;}}{\;}$2CaO+2SO2↑+O2↑.
故答案为:2CaSO4•H2O,2CaSO4$\frac{\underline{\;高温\;}}{\;}$2CaO+2SO2↑+O2↑.
点评 本题全面考查了学生对知识的掌握和应用能力,难度比较大,解答时一定要注意知识的前后的联系和综合运用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.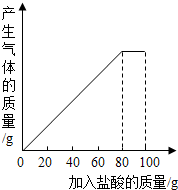 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应,也不溶于水),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应,也不溶于水),得到如下部分数据和图象.
请计算:
(1)第2次加入盐酸后,a为25g.
(2)石灰石样品中钙元素、碳元素和氧元素的质量比为多少?10:3:22.
(3)求所用盐酸的质量分数?
 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应,也不溶于水),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应,也不溶于水),得到如下部分数据和图象.| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
(1)第2次加入盐酸后,a为25g.
(2)石灰石样品中钙元素、碳元素和氧元素的质量比为多少?10:3:22.
(3)求所用盐酸的质量分数?
3.世界卫生组织(WHO)提出的空气质量指标如下表所示:(达到指标值可认为被空气污染,超过指标值为较重污染),已知成年人每天吸入空气约为14m3.计算:
(1)从上表中可知二氧化硫指标每立方米超过400×10-6g可认为空气被较重污染.
(2)每个成年人在没被污染的空气中,每天吸入氧气的体积约为2.9或2.8立方米(精确到0.1).
| 污染物 | 指标/10-6gm-3 | 污染物 | 指标/10-6gm-3 | |
| 二氧化硫 | 5-400 | 二氧化氮 | 10-150 | |
| 一氧化碳 | 500-700 | 铅 | 0.01-2 |
(2)每个成年人在没被污染的空气中,每天吸入氧气的体积约为2.9或2.8立方米(精确到0.1).
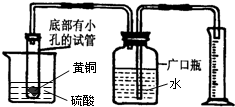 黄铜是铜与锌的合金,因色黄而得名.黄铜的机械性能和耐磨性能都很好,可用于制造精密仪器、船舶的零件、枪炮的弹壳等.
黄铜是铜与锌的合金,因色黄而得名.黄铜的机械性能和耐磨性能都很好,可用于制造精密仪器、船舶的零件、枪炮的弹壳等.