题目内容
金属材料在生活、生产中应用非常广泛,请仔细看图并填空:
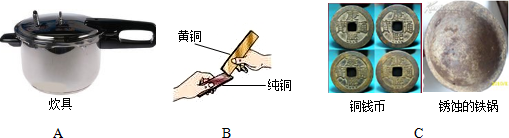
(1)图A主要是利用了金属的 性.
(2)图B是用两块金属片相互刻划,观察到在纯铜片上有明显的划痕.该实验探究的目的是 .
(3)2010年5月,400多年前的古沉船“南澳一号”成功打捞.图C是古船上部分文物图片,其中可以判断铁比铜活泼的信息是 .稀盐酸除锈的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O,该反应的基本类型为 .生活中常用的防锈方法有 .
(4)为了比较铁和铜的活动性,小华选用了硫酸铜溶液.请你写出该反应的化学方程式 .

(1)图A主要是利用了金属的
(2)图B是用两块金属片相互刻划,观察到在纯铜片上有明显的划痕.该实验探究的目的是
(3)2010年5月,400多年前的古沉船“南澳一号”成功打捞.图C是古船上部分文物图片,其中可以判断铁比铜活泼的信息是
(4)为了比较铁和铜的活动性,小华选用了硫酸铜溶液.请你写出该反应的化学方程式
考点:金属的物理性质及用途,合金与合金的性质,金属锈蚀的条件及其防护,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:根据金属的性质进行分析,金属具有导热性,可用于炊具,合金的硬度比纯金属大,铁的活动性比铜强,盐酸能与氧化铁反应,能与硫酸铜反应生成硫酸亚铁和铜.
解答:解:
(1)金属制成炊具主要是利用了金属u的导热性,所以本题答案为:导热;
(2)使用纯铜与黄铜互相刻划,主要是想探究纯金属与合金的硬度,所以本题答案为:探究纯金属与合金的硬度;
(3)根据金属的锈蚀程度可以断定铁的活动性比铜强,铁锅锈蚀比铜严重;盐酸能与氧化铁反应生成氯化铁和水,反应的方程式为:Fe2O3+6HCl═2FeCl3+3H2O,符合两种化合物相互交换成分,生成另外两种化合物的反应,属于复分解反应;要防锈就是使铁与水或氧气隔绝,可以在金属表面覆盖保护层,
(4)铁能与硫酸铜反应生成硫酸亚铁和铜,所以本题答案为:Fe+CuSO4═Cu+FeSO4.
答案:
(1)导热
(2)探究纯金属与合金的硬度
(3)铁锅锈蚀比铜严重 复分解反应 覆盖保护层
(4)Fe+CuSO4═Cu+FeSO4
(1)金属制成炊具主要是利用了金属u的导热性,所以本题答案为:导热;
(2)使用纯铜与黄铜互相刻划,主要是想探究纯金属与合金的硬度,所以本题答案为:探究纯金属与合金的硬度;
(3)根据金属的锈蚀程度可以断定铁的活动性比铜强,铁锅锈蚀比铜严重;盐酸能与氧化铁反应生成氯化铁和水,反应的方程式为:Fe2O3+6HCl═2FeCl3+3H2O,符合两种化合物相互交换成分,生成另外两种化合物的反应,属于复分解反应;要防锈就是使铁与水或氧气隔绝,可以在金属表面覆盖保护层,
(4)铁能与硫酸铜反应生成硫酸亚铁和铜,所以本题答案为:Fe+CuSO4═Cu+FeSO4.
答案:
(1)导热
(2)探究纯金属与合金的硬度
(3)铁锅锈蚀比铜严重 复分解反应 覆盖保护层
(4)Fe+CuSO4═Cu+FeSO4
点评:本题考查了金属的性质,完成此题,可以依据已有的金属的性质进行.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
下列对有关实验现象的描述错误的是( )
| A、铁丝在氧气中燃烧时,火星四射,有黑色物质生成 |
| B、硫在氧气中燃烧,发出明亮的蓝紫色火焰 |
| C、石蜡在空气中燃烧时,生成水和二氧化碳 |
| D、木炭在氧气中燃烧发出白光 |
人类为了维持生命和健康,必须摄取食物.下列说法不正确的是( )
| A、猪肉、牛肉含丰富的蛋白质 |
| B、花生油、牛油属于油脂 |
| C、水果、蔬菜含有丰富的维生素 |
| D、稻子、马铃薯不属于糖类 |
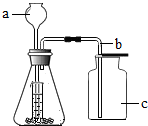 如图是某同学设计的实验室制取气体的装置,请你回答下列问题:
如图是某同学设计的实验室制取气体的装置,请你回答下列问题: