题目内容
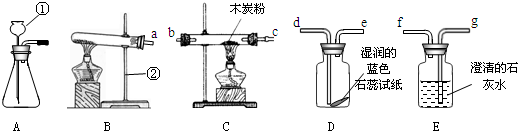
6.利用下列所示仪器、药品(及其他必要物品)(A-H)进行实验并探究.
供选药品:高锰酸钾、石灰石、二氧化锰、过氧化氢溶液、稀盐酸五种药品.
(1)小林制取二氧化碳时,选用的药品是石灰石、稀盐酸,收集的方法是向上排空气法.向试管中加入2mL蒸馏水,滴入1~2滴石蕊溶液,先向其中通入二氧化碳,将通入二氧化碳的试管放在酒精灯上加热,(如图甲所示)加热时试管中发生的化学反应方程式是H2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑.
(2)小江制取并收集氧气,选用了过氧化氢溶液和二氧化锰.
①选用的仪器是除了E和H外,还需要的是试管、集气瓶(填仪器名称),生成氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②如果想得到平稳的氧气流,可以增加的仪器是D(填序号),具体的操作是B.
A.把二氧化锰缓缓加入装有过氧化氢溶液的试管中
B.把过氧化氢溶液缓缓加入装有二氧化锰的试管中
③若消耗了17g的5%的过氧化氢溶液,充分反应后,理论上可得氧气的质量为0.4g.
④小芬建议改用图乙的装置进行实验,对比分析该装置的优点:反应产生较大量氧气或可以随时添加试剂(只写一点).
(3)如果想用高锰酸钾制取氧气时,此时还需要补充的实验仪器为酒精灯.
分析 (1)根据实验室中制取二氧化碳的原理、收集方法、以及碳酸不稳定来分析;
(2)根据反应的原理和实验要求来分析实验仪器的选择;
根据化学方程式,利用过氧化氢的质量来计算生成氧气的质量;
根据装置的特点来分析;
(3)高锰酸钾是在加热的条件下分解产生氧气.
解答 解:(1)在实验室中,通常用大理石或石灰石与稀盐酸反应来制取二氧化碳,因为二氧化碳的密度比空气大且能溶于水,故用向上排空气法来收集;二氧化碳能与水反应生成碳酸,在加热的条件下,碳酸会分解为水和二氧化碳;故填:石灰石、稀盐酸;向上排空气法;H2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑;
(2)①用过氧化氢溶液和二氧化锰来制取氧气,需要试管、铁架台、集气瓶、导气管等;在二氧化锰的催化作用下,过氧化氢分解为水和氧气;故填:试管;集气瓶;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
②要得到平稳的氧气流则须控制反应物的流速,注射器可达到此目的;故填:D;B;
③解:设理论上可得氧气的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
17g×5% x
$\frac{68}{32}=\frac{17g×5%}{x}$
x=0.4g
故填:0.4;
④该装置容积较大,且使用了长颈漏斗,便于随时添加液体试剂;故填:反应产生较大量氧气或可以随时添加试剂(只写一点);
(3)高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气,所以需要酒精灯;故填:酒精灯.
点评 明确常用仪器,制取二氧化碳和氧气的方法和装置选取依据等知识,即可结合题意顺利解答.

| A. | 氯化氢 | B. | 氢气 | C. | 硫酸铜 | D. | 汞 |
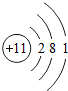 ,能够获得的信息是( )
,能够获得的信息是( )①反应中得失电子数目 ②相对原子质量 ③原子的质子数 ④元素的化学性质.
| A. | ②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
| A. | 稀HCl滴入Ba(OH)2溶液中 | B. | K2CO3溶液加入到H2SO4溶液中 | ||
| C. | Fe2O3加入到NaOH溶液中 | D. | Na2SO4溶液加入到Ba(NO3)2溶液中 |
| A. | 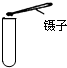 取用块状固体 | B. | 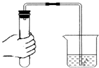 检查装置气密性 | C. | 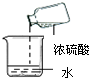 稀释浓硫酸 | D. | 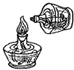 点燃酒精灯 |
| A. | 冰融为水 | B. | 矿石粉碎 | C. | 食物腐败 | D. | 山体滑坡 |
| A. | 60℃时50 g水中加入60g KNO3得105g饱和溶液则60℃时KNO3的溶解度是110g | |
| B. | 20℃时向20g饱和石灰水中加入少量生石灰,恢复到20℃时溶液中溶质的质量减小 | |
| C. | 硝酸钾的饱和溶液中含少量氯化钠时,可以通过冷却热饱和溶液的方法提纯硝酸钾 | |
| D. | 对固体溶质而言,温度不变时溶液从不饱和变成饱和,其质量分数不一定增大 |