题目内容
4.下列有关实验现象解释正确的是( )| A. | 淀粉溶液中加碘水后溶液变监,说明淀粉与碘的化合物作用生成蓝色物质 | |
| B. | 浓盐酸打开瓶盖后有大量白雾,该白雾就是从浓盐酸中挥发出来的氯化氢 | |
| C. | 水银温度计中的水银柱会随温度升高而升高,说明升温后微粒间距会增大 | |
| D. | 用盐酸浸泡生锈的铁钉后溶液呈黄色,说明反应生成的氯化亚铁是黄色的 |
分析 A、根据碘遇淀粉变蓝色的特性,进行分析判断.
B、根据浓盐酸具有挥发性,进行分析判断.
C、水银是金属汞的俗称,是由汞原子直接构成的,结合原子的基本性质进行分析判断.
D、根据铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,进行分析判断.
解答 解:A、碘遇淀粉变蓝色,淀粉溶液中加碘水后溶液变监,说明淀粉与碘作用生成蓝色物质,故选项解释错误.
B、浓盐酸具有挥发性,打开瓶盖后有大量白雾,该白雾就是从浓盐酸中挥发出来的氯化氢与空气中的水蒸气结合成的盐酸小液滴,故选项解释错误.
C、水银是金属汞的俗称,是由汞原子直接构成的,水银温度计中的水银柱会随温度升高而升高,说明升温后微粒间距会增大,故选项解释正确.
D、铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,生成的氯化铁溶液呈黄色,故选项解释错误.
故选:C.
点评 本题难度不大,掌握碘遇淀粉变蓝色的特性、浓盐酸具有挥发性、利用微粒的基本性质分析和解决问题的方法、酸的化学性质是正确解答本题的关键.

练习册系列答案
相关题目
5.洗发水中一般含有少许二恶烷(化学式是C4H8O2),二恶烷主要用作溶剂、乳化剂、去垢剂等.下列有关二恶烷的说法正确的是( )
| A. | 二恶烷属于有机高分子化合物 | |
| B. | 二恶烷中含有4个碳原子、8个氢原子和2个氧原子 | |
| C. | 二恶烷中碳元素的质量分数约是54.5% | |
| D. | 二恶烷中碳、氢、氧三种元素的质量比是2:4:1 |
12.摩尔(符号:mol)是物质的量的单位.1mol任何物质的质量以克为单位时,在数值上都与其相对分子质量相等,如:1mol H2O的质量为18克;标准状况下,1mol任何气体的体积为22.4升.则标准状况下,33.6升甲烷的质量是( )克.
| A. | 16 | B. | 24 | C. | 32 | D. | 40 |
19.如图是甲、乙两种物质的溶解度曲线,则下列叙述正确的是( )
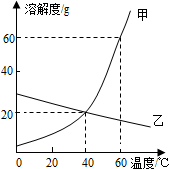

| A. | 50℃时,甲物质的溶解度大于乙物质的溶解度 | |
| B. | 40℃时,甲、乙两物质溶液的溶质质量分数一定相等 | |
| C. | 升高温度可以将乙的饱和溶液转化为不饱和溶液 | |
| D. | 可用100g水配制60℃时溶液质量为180g的甲溶液 |
14.20℃时,取甲、乙、丙、丁四种纯净物各20g,分别加入到四个各盛有50g水的烧杯中,充分溶解,其溶解情况如下表:
下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 未溶解固体的质量/g | 4.2 | 2 | 0 | 9.2 |
| A. | 所得溶液一定都是饱和溶液 | |
| B. | 20℃时四种物质溶解度的关系为:丁>甲>乙>丙 | |
| C. | 丁溶液中溶质质量分数一定最大 | |
| D. | 所得溶液的质量关系为:丙>乙>甲>丁 |
 A,B,C,D,E是初中化学中常见的五种物质,它们都含有一种相同的元素,如图表示各物质的转化关系.其中,A为食盐的主要成分,B中含钡元素,D为有颜色溶液,E为蓝色溶液,其它物质的溶液都为无色;反应⑤和⑥为置换反应,其它均为分解反应.(1)写出物质C的化学式HCl.
A,B,C,D,E是初中化学中常见的五种物质,它们都含有一种相同的元素,如图表示各物质的转化关系.其中,A为食盐的主要成分,B中含钡元素,D为有颜色溶液,E为蓝色溶液,其它物质的溶液都为无色;反应⑤和⑥为置换反应,其它均为分解反应.(1)写出物质C的化学式HCl. 根据图回答问题.
根据图回答问题.