题目内容
20. 金属用途广泛,如图为某学习小组探究金属化学性质时所做实验,仔细分析后回答下列问题:
金属用途广泛,如图为某学习小组探究金属化学性质时所做实验,仔细分析后回答下列问题:(1)铝比铁活泼,但为什么铝在空气中却表现出良好的抗腐蚀性?
(2)写出A中反应的化学反应方程式
(3)请描述B中的实验现象
(4)两只试管中发生的反应可以证明相关金属的活动性顺序是什么?
分析 (1)依据铝与氧气反应生成的氧化铝的性质分析回答;
(2)根据铜和硝酸银反应产生硝酸铜和银写出反应的方程式;
(3)根据铁和硫酸铜反应产生的铜和硫酸亚铁描述现象;
(4)根据金属和盐溶液反应的规律分析:只有前面的金属可以把排在它后面的金属从盐溶液中置换出来.
解答 解:(1)铝的化学性质较活泼在空气中能与氧气反应生成氧化铝,氧化铝覆盖在铝表面,起到了保护里层的金属铝的作用;
故填:铝和氧气反应生成了致密的氧化铝薄膜,覆盖在铝表面,保护了里层的金属铝;
(2)铜与硝酸银反应生成硝酸铜溶液和银,故反应的化学方程式为:Cu+2AgNO3=Cu(NO3)2+2Ag;
(3)由于在金属活动性顺序中铁的活动性大于铜的活动性,所以铁能与硫酸铜发生置换反应生成硫酸亚铁和铜,硫酸亚铁的水溶液为浅绿色,铜为红色,故铁丝上附有红色固体,溶液由蓝色变为浅绿色;故填:铁丝上附有红色固体,溶液由蓝色变为浅绿色;
(4)由A知铜能置换出硝酸银中的银,说明活动性铜>银,B中的铁能置换出硫酸铜中的铜,说明活动性铁>铜,所以可得活动性:铁>铜>银;故填:铁>铜>银.
点评 本题以实验探究为主题,主要考查了金属的化学性质,要求学生要具有利用金属活动顺序的意义设计实验、分析实验的能力.

练习册系列答案
相关题目
11.下列反映中,属于分解反应的是( )
| A. | 用加热氯酸钾和二氧化锰的混合物的方法制氧气 | |
| B. | 甲烷在空气中燃烧 | |
| C. | 细铁丝在氧气中燃烧 | |
| D. | 石灰石和稀盐酸反应 |
5.下列操作或现象与分子特性对应关系不正确的是( )
| 选项 | 操作或现象 | 分子特性 |
| A | 气体可压缩储存于钢瓶中 | 分子间有间隙 |
| B | 物体的热胀冷缩 | 分子的大小是可以变化的 |
| C | 湿衣服晾干 | 分子是运动的 |
| D | 1滴水中大约有1.67×1021个水分子 | 分子很小 |
| A. | A | B. | B | C. | C | D. | D |
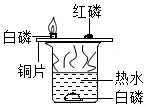 已知白磷的着火点为40℃,红磷的着火点为240℃.如图所示,回答下列问题:
已知白磷的着火点为40℃,红磷的着火点为240℃.如图所示,回答下列问题:
 据中青网报道,在山东东营利津县城附近,不少村民用6米长的塑料袋灌装天然气带回家,令不少路人为此举捏汗.路人称,这样带着天然气回家存在着较大的安全隐患.其中天然气的主要成分是( )
据中青网报道,在山东东营利津县城附近,不少村民用6米长的塑料袋灌装天然气带回家,令不少路人为此举捏汗.路人称,这样带着天然气回家存在着较大的安全隐患.其中天然气的主要成分是( )