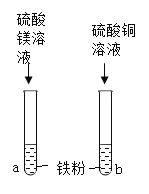
题目内容
如下图1是已学的获得氧气的六种途径,根据装置图回答问题。

(1)写出B中的仪器名称:①_________。
(2)若要通过途径a制取较干燥的氧气,可选择的发生与收集装置为_____,反应的化学方程式为______。若收集O2实验中始终未能检验到O2已集满,可能的原因是______。
(3)根据“绿色化学”理念,途径________(填字母)是实验室制氧气的最佳方法。
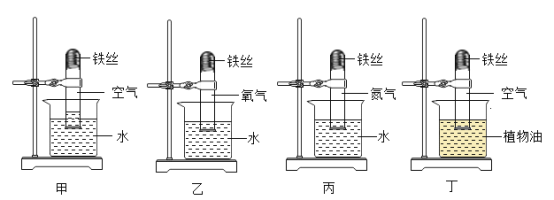
(4)铁在氧气中燃烧的现象为___________,该反应的化学方程式为_______。铁在空气中无法燃烧,但在潮湿的空气中会发生缓慢氧化。以下四种情况,锈蚀最严重的是_________。
(5)固体氢化钙(CaH2)常温下能与水反应生成H2,是野外工作人员便携燃料的来源。若实验室利用氢化钙制取氢气,选择的发生和收集装置为______。
小亮同学想通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题. 他设计并完成了下表所示的探究实验:
(1)请你帮小明同学填写上表中未填完的空格;
实验操作 | 实验现象 | 实验结论或总结 | ||
各步骤结论 | 总结 | |||
实验一 | 取5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是_____, 文字表达式为:_____, | 二氧化锰是过氧化氢分解的催化剂 |
实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | _____, | |
实验三 | _____, | _____, | 二氧化锰能加快过氧化氢的分解 |
(2)在小明的探究实验中,实验一和实验二起的作用是_____。
(3)小米同学认为仅由上述实验还不能完全得出表内“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明。
第一方面的实验操作是将实验三反应前和反应后的二氧化锰进行称量,其目的是:_____,
第二方面的实验是_____,其目的是验证二氧化锰在化学反应前后化学性质不变。
某中学化学兴趣小组通过实验测定某大理石中碳酸钙的质量分数。将盛有一定量该样品的烧杯放在电子秤上,倒入100.0g稀盐酸(假设大理石样品中的杂质不与稀盐酸反应,也不溶于水),使该样品完全反应,已知烧杯的质量为60.0g,实验过程中的有关数据如下表:
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
烧杯与所盛物质质量/g | 186.0 | 183.0 | 181.0 | 180.0 | 179.4 | 179.4 |
试计算:
(1)碳酸钙中碳元素与氧元素的质量比(最简比)为_________。
(2)生成二氧化碳的质量为_________g。
(3)求该大理石中碳酸钙的质量分数___________(精确到0.1%)。


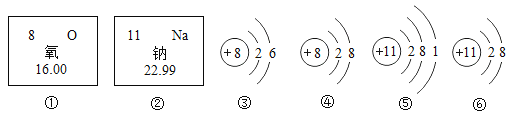
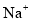 的结构示意图是
的结构示意图是
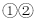 两种元素可组成化学式为
两种元素可组成化学式为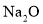 的化合物
的化合物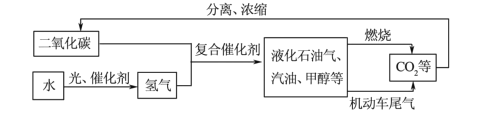
 与
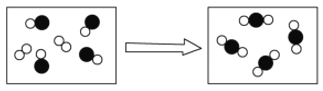
与 分别代表不同元素原子),该反应可能为( )
分别代表不同元素原子),该反应可能为( )