题目内容
1.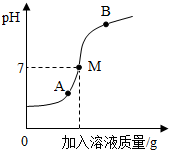 如图是氢氧化钠溶液与稀硫酸反应时,溶液的pH变化曲线图.下列说法正确的是( )
如图是氢氧化钠溶液与稀硫酸反应时,溶液的pH变化曲线图.下列说法正确的是( )| A. | 该实验是将稀硫酸滴入氢氧化钠溶液中 | |
| B. | 曲线上A点的溶液里溶质有H2SO4、Na2SO4和NaOH | |
| C. | 取曲线上M点的溶液,向其中滴入无色酚酞试液,溶液变红色 | |
| D. | 曲线上B点的溶液里溶质有两种 |
分析 A、根据当溶液的pH<7时,溶液显酸性,当溶液的pH>7时,溶液显碱性,当溶液的pH=7时,溶液显中性解答;
B、根据A点pH<7,硫酸过量解答;
C、根据M点溶液的pH=7,溶液为中性解答;
D、根据A点pH>7,氢氧化钠过量以及反应原理以及图象数据来回答.
解答 解:A、根据图象,在反应未进行时,溶液的pH<7,为强酸性溶液,所以该曲线反应是将氢氧化钠溶液滴入硫酸中,故错;
B、硫酸能与氢氧化钠反应生成硫酸钠和水,当加入的溶液质量为ag时,溶液的pH小于7,显酸性,故溶液中除了硫酸钠还有没参加反应的硫酸,故错;
C、M点溶液的pH=7,溶液为中性,向其中滴入无色酚酞试液,溶液变无色,故错;
D、当B时,pH>7,溶液为碱性,所得溶液中的溶质有生成的硫酸钠也有剩余的氢氧化钠.故对;
故选:D.
点评 酸碱中和反应结合图象知识来考查,难度适中,考查的知识面较广.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
11.小亮同学在实验室中制取CO2气体后,对废液进行后续探究,他向一定质量的含CaCl2和HCl的废液中逐滴加入溶质质量分数为10%的Na2CO3溶液.实验过程中加入Na2CO3溶液质量与产生沉淀或气体的质量关系如图1所示;加入Na2CO3溶液的质量与溶液的PH变化关系如图2所示,下列说法正确的是( )
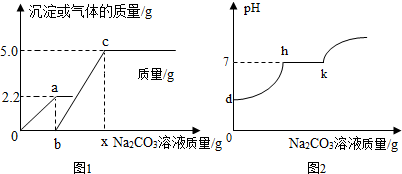

| A. | 图1中b→c段表示生成气体的过程 | |
| B. | 图1中b点的值为53 | |
| C. | 图1中c时,溶液中的溶质有两种 | |
| D. | 图1中o→a段反应过程中溶液的PH变化情况可用图2中h→k段表示 |
13.小敏和小玉在实验室用盐酸和石灰石反应,分别用甲、乙装置(气密性均良好)进行二氧化碳的制取及性质实验,但均未发现澄清石灰水边浑浊.针对此现象,同学们提出了自己的想法.小敏同学实验时澄清石灰水未变浑浊的原因是产生的气体从长颈漏斗中逸出.
【提出问题】小玉同学实验时澄清石灰水为什么没有变浑浊呢?
【作出猜想】猜想一:澄清石灰水变质.猜想二:反应产生的气体除了有二氧化碳外,还有氯化氢.
【查阅资料】氯化氢气体溶于水形成盐酸.
【实验探究】

同学们经过讨论发现,用丙装置(如图)在A、B中均加入实验Ⅱ所用试剂即可同时完成上述两个猜想的探究,其中B装置所起的作用是检验氯化氢气体是否除尽.如果看到A中有白色沉淀产生,B,C中无变化的现象,则两个猜想都成立.
【实验反思】由实验可知,小玉同学实验时可能错误使用了一种药品,她使用的药品是浓盐酸.
【提出问题】小玉同学实验时澄清石灰水为什么没有变浑浊呢?
【作出猜想】猜想一:澄清石灰水变质.猜想二:反应产生的气体除了有二氧化碳外,还有氯化氢.
【查阅资料】氯化氢气体溶于水形成盐酸.
【实验探究】

| 实验 | 实验步骤 | 实验现象 | 实验结论 |
| 实验Ⅰ | 将纯净的CO2通入到该实验所用的澄清石灰水中 | 澄清的石灰水边浑浊 | 猜想一不成立 |
| 实验Ⅱ | 将反应产生的气体通入到硝酸银溶液中 | 有白色沉淀产生 | 猜想二成立 |
【实验反思】由实验可知,小玉同学实验时可能错误使用了一种药品,她使用的药品是浓盐酸.
12.实验室配制100g10%的氯化钠溶液,有关实验操作不正确的是( )
| A. | 用托盘天平称取10.0g氯化钠 | |
| B. | 用100mL量筒量取90.0mL 水 | |
| C. | 将称取的氯化钠倒入量筒中搅拌溶解 | |
| D. | 将配制好的溶液装入试剂瓶中,贴上标签 |
 化学与生活密切相关.
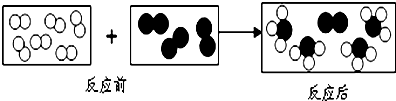
化学与生活密切相关.
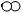 ”和“
”和“ ”分别代表两种不同的单质分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如图:
”分别代表两种不同的单质分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如图: