题目内容
4.一定量的氧气和甲烷反应,测得反应前后各物质的质量如下表,则下列有关说法正确的是( )| 物质 | 氧气 | 甲烷 | 水 | 二氧化碳 | X |
| 反应前质量/g | 11.2 | 3.2 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 4.4 | 待测 |
| A. | 反应类型属于分解反应 | |
| B. | X中两种元素的质量比为1:1 | |
| C. | 反应后X的质量为3.6g | |
| D. | 反应方程式中氧气与水的化学计量数之比为7:8 |
分析 反应后甲烷质量减少3.2g,是反应物;
反应后氧气质量减少11.2g,是反应物;
反应后水的质量增加7.2g,是生成物;
反应后二氧化碳质量增加4.4g,是生成物;
根据质量守恒定律可知,X是生成物,生成的质量为:11.2g+3.2g-7.2g-4.4g=2.8g.
解答 解:A、反应物是两种,生成物是三种,不属于分解反应,该选项说法错误;
B、甲烷中氢元素质量是3.2g×$\frac{4}{16}$×100%=0.8g,碳元素的质量是3.2g-0.8g=2.4g,
7.2g水中氢元素的质量为:7.2g×$\frac{2}{18}$×100%=0.8g,氧元素质量为:7.2g-0.8g=6.4g,
4.4g二氧化碳中氧元素的质量为:4.4g×$\frac{32}{44}$×100%=3.2g,碳元素的质量是4.4g-3.2g=1.2g,
则X中氧元素的质量为:11.2g-3.2g-6.4g=1.6g,所以X中不含氢元素,X中含有碳元素的质量是2.4g-1.2g=1.2g,故X中两种元素的质量比为1.6:1.2≠1:1,该选项说法错误;
C、根据质量守恒定律可知,X是生成物,生成的质量为:11.2g+3.2g-7.2g-4.4g=2.8g,该选项说法错误;
D、由题意可知:反应中氧气和水的计量水之比:$\frac{11.2g}{32}:\frac{7.2g}{18}$=7:8,该选项说法正确.
故选:D
点评 本题考查学生利用表格中物质的质量及质量守恒来分析生成物,明确化学反应方程式中物质恰好完全反应的质量比及元素质量的计算是解答的关键.

练习册系列答案
相关题目
11.下列溶液中的离子能大量共存的是( )
| A. | Na+、K+、OH-、SO42- | B. | Na+、Ba2+、OH-、SO42- | ||
| C. | Na+、Mg2+、SO42-、OH- | D. | Ca2+、SO42-、NO3-、CO32- |
9.下列几种物质中,加点元素的化合价为+2价的是( )
| A. | K$\underset{Mn}{•}$O4 | B. | Na2$\underset{S}{•}$2O3 | C. | H2$\underset{C}{•}$2O4 | D. | Na2$\underset{Fe}{•}$O4 |
16.下列各组物质中所含分子数相同的是( )
| A. | 1gH2和8gO2 | B. | 0.1mol HCl和2.24L氯化氢 | ||
| C. | 28gCO和22gCO2 | D. | 9gH2O和0.5molCO2 |
14.已知木炭还原氧化铜实验中发生的主要反应:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,某化学兴趣小组对该实验红色固体产物的成份(假设反应物已完全反应)作如下探究:
探究一:检验红色固体产物的成份
【查阅资料】Ⅰ.木炭还原氧化铜除生成铜外还可能生成氧化亚铜(Cu2O);
Ⅱ.Cu和Cu2O均为不溶于水的红色固体;Ⅲ.Cu2O+H2SO4═CuSO4+Cu+H2O
【提出问题】该实验的红色固体产物中含有什么物质?
【猜想与假设】假设1:红色固体只含Cu; 假设2:红色固体只含Cu2O;
假设3:红色固体Cu、Cu2O的混合物(请补充完成假设3).
【实验探究】(填写表中空格)
探究二:测定该实验红色固体产物中Cu2O的含量
该化学兴趣小组经交流讨论后,设计了如下两方案:
方案一:称取5.00g红色固体加入到足量稀硫酸溶液中使其充分反应后,操作A、洗涤、干燥,称量得红色固体质量为4.10g.
(1)操作A的名称是过滤,在实验室中完成操作A的玻璃仪器有玻璃棒、烧杯和漏斗;
(2)检验反应后剩余红色固体是否洗涤干净的方法是:取少量最后一次洗涤液,加入氢氧化钠溶液,如果观察到现象:无蓝色沉淀生成,说明已洗涤干净.
(3)通过计算,假设3成立,红色固体产物中Cu2O的含量为1.44g;
方案二:称取5.00g的红色固体,用如图所示装置进行实验(固定装置略去,碱石灰为氧化钙和氢氧化钠的混合物),通过测定反应前后装置d的质量达到实验目的.
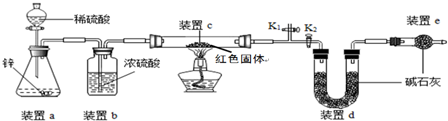
(1)装置a中用稀硫酸而不用稀盐酸,原因是盐酸挥发出氯化氢气体,与d中的物质反应,影响测定结果;
(2)装置b的作用是干燥氢气,若不加装置b,实验结果会偏大(“偏大”或“偏小”);
(3)装置c中涉及的反应化学方程式Cu2O+H2$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+H2O;
(4)装置e的作用是防止空气中CO2及H2O对装置d的测量造成误差,若不加装置e,实验结果会偏大(“偏大”或“偏小”);
(5)点燃酒精灯前涉及的部分操作如下,
①连接仪器;②检查装置的气密性;
③关闭K2,打开K1,通氢气一段时间以赶尽装置内原有的空气,其目的是:a.防止空气中的H2O和CO2进入装置d干扰测定;b.防氢气不纯,发生爆炸,检验空气是否赶尽的方法是:在K1处用小试管收集气体,进行点燃;④打开K2,关闭K1
(6)经测定反应前后装置d的质量分别为100.00g、100.18g,计算产物中Cu2O的含量(写出计算过程,最后结果保留小数点后1位)
【交流与反思】
(1)在方案一实验测定中,若测定结果偏大,则下列可能的原因有①②③.(填序号)
①反应后剩余红色固体未洗涤干净 ②洗涤后未完全干燥
③干燥方法采用的是在空气中加热烘干 ④称量剩余红色固体时,有部分固体洒落到实验台上
(2)方案二中利用同样的装置,还可通过测定反应前后装置c(填“a”、“b”或“c”)的质量达到实验目的.
探究一:检验红色固体产物的成份
【查阅资料】Ⅰ.木炭还原氧化铜除生成铜外还可能生成氧化亚铜(Cu2O);
Ⅱ.Cu和Cu2O均为不溶于水的红色固体;Ⅲ.Cu2O+H2SO4═CuSO4+Cu+H2O
【提出问题】该实验的红色固体产物中含有什么物质?
【猜想与假设】假设1:红色固体只含Cu; 假设2:红色固体只含Cu2O;
假设3:红色固体Cu、Cu2O的混合物(请补充完成假设3).
【实验探究】(填写表中空格)
| 实验操作 | 实验现象 | 实验结论 |
| 取少量红色固体加入到足量稀硫酸溶液中 | 若无明显现象 | 假设1成立 |
| 若固体部分(选填“全部”或“部分”)溶解,溶液由无色变蓝色 | 假设2和假设3均成立 |
该化学兴趣小组经交流讨论后,设计了如下两方案:
方案一:称取5.00g红色固体加入到足量稀硫酸溶液中使其充分反应后,操作A、洗涤、干燥,称量得红色固体质量为4.10g.
(1)操作A的名称是过滤,在实验室中完成操作A的玻璃仪器有玻璃棒、烧杯和漏斗;
(2)检验反应后剩余红色固体是否洗涤干净的方法是:取少量最后一次洗涤液,加入氢氧化钠溶液,如果观察到现象:无蓝色沉淀生成,说明已洗涤干净.
(3)通过计算,假设3成立,红色固体产物中Cu2O的含量为1.44g;
方案二:称取5.00g的红色固体,用如图所示装置进行实验(固定装置略去,碱石灰为氧化钙和氢氧化钠的混合物),通过测定反应前后装置d的质量达到实验目的.

(1)装置a中用稀硫酸而不用稀盐酸,原因是盐酸挥发出氯化氢气体,与d中的物质反应,影响测定结果;
(2)装置b的作用是干燥氢气,若不加装置b,实验结果会偏大(“偏大”或“偏小”);
(3)装置c中涉及的反应化学方程式Cu2O+H2$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+H2O;
(4)装置e的作用是防止空气中CO2及H2O对装置d的测量造成误差,若不加装置e,实验结果会偏大(“偏大”或“偏小”);
(5)点燃酒精灯前涉及的部分操作如下,
①连接仪器;②检查装置的气密性;
③关闭K2,打开K1,通氢气一段时间以赶尽装置内原有的空气,其目的是:a.防止空气中的H2O和CO2进入装置d干扰测定;b.防氢气不纯,发生爆炸,检验空气是否赶尽的方法是:在K1处用小试管收集气体,进行点燃;④打开K2,关闭K1
(6)经测定反应前后装置d的质量分别为100.00g、100.18g,计算产物中Cu2O的含量(写出计算过程,最后结果保留小数点后1位)
【交流与反思】
(1)在方案一实验测定中,若测定结果偏大,则下列可能的原因有①②③.(填序号)
①反应后剩余红色固体未洗涤干净 ②洗涤后未完全干燥
③干燥方法采用的是在空气中加热烘干 ④称量剩余红色固体时,有部分固体洒落到实验台上
(2)方案二中利用同样的装置,还可通过测定反应前后装置c(填“a”、“b”或“c”)的质量达到实验目的.
 托盘天平是一种实验室常用的称量用具,请回答下列问题:
托盘天平是一种实验室常用的称量用具,请回答下列问题: