题目内容
4.硅-一种重要的半导体材料,应用范围广.三氯苯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图所示:
(1)硅属于非金属(填“金属”或“非金属”)元素;
(2)写出上述流程中一种氧化物的化学式SiO2;
(3)上述流程中最后一步反应的化学方程式为SiHCl+H2$\frac{\underline{\;高温\;}}{\;}$Si+3HCl,该反应属于置换反应(基本反应类型);
(4)如果还原SiHCl过程中混入O2,可能引起的后果是爆炸.
(5)该流程中可以循环利用的物质的化学式是HCl.
分析 (1)根据元素的名称分析类别;
(2)根据物质的组成分析属于氧化物的物质,写出化学式;
(3)分析流程中最后一步发生的反应写出发生的化学方程式,根据反应的特点分析类型;
(4)根据氢气和氧气的混合气体点燃时易发生爆炸分析回答;
(5)根据流程分析可以循环利用的物质.
解答 解:(1)硅的名称中带有“石”字旁,属于非金属;
(2)二氧化硅是由硅元素和氧元素组成的,属于氧化物,化学式为SiO2;
(3)上述流程中最后一步反应的化学方程式为:SiHCl+H2$\frac{\underline{\;高温\;}}{\;}$Si+3HCl,该反应由一种单质与一种化合物反应,生成了另一种单质和另一种化合物,属于置换反应;
(4)如果还原SiHCl过程中混入O2,会形成氢气和氧气混合气体,点燃时易引起爆炸.
(5)该流程中可以循环利用的物质的化学式是HCl.
故答为:(1)非金属;(2)SiO2;(3)SiHCl+H2$\frac{\underline{\;高温\;}}{\;}$Si+3HCl,置换反应(4)爆炸;(5)HCl.
点评 此题主要是考查学生的综合分析能力,不但要求学生具备有关物质的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.

练习册系列答案
相关题目
8.下列过程中没有发生化学变化的是( )
| A. | 从铝土矿(主要成化是Al2O3)中提煤炼金属铝 | |
| B. | 秸秆、杂草、粪便等在沼气池中发酵 | |
| C. | 二氧化碳气体经加压、降温得到干冰 | |
| D. | 排放到空气中的二氧化硫形成酸雨 |
12.空气是人类宝贵的自然资源,下列关于空气中各成分的说法不正确的是( )
| A. | 氧气化学性质活泼,常用于作燃料 | |
| B. | 氮气化学性质稳定,是制造硝酸和氮肥的重要原料 | |
| C. | 稀有气体在通电时能发出不同颜色的光,可制五光十色的霓虹灯 | |
| D. | 二氧化碳升华吸热,干冰常用于人工降雨 |
19.下列物品所使用的主要材料属于有机合成材料的是( )
| A. | 纯棉衣服 | B. | 玻璃棒 | C. | 羊毛围巾 | D. | 胶皮手套 |
16.KCl和KNO3是两种常见的化肥肥料,它们在不同温度时的溶解度如下表,请回答下列问题.
(1)KNO3作为化学肥料,其中营养元素是N、K20℃时,KNO3的溶解度是31.6g.
(2)KCl和KNO3的溶解度相等时的温度范围是20℃-30℃℃.
(3)用50g蒸馏水配制40℃时KCl的饱和溶液,需KCl固体质量是20g,操作步骤是:计算、称量溶解.
(4)将40℃时KCl的饱和溶液与KNO3的饱和溶液个100g降温至10℃,对所得溶液的描述正确的是AC(填序号)
A.都是饱和溶液 B.溶液质量:KCl<KNO3 C.溶剂重量:KCl>KNO3.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 |
| KCl的溶解度/g | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 |
| KNO3的溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 |
(2)KCl和KNO3的溶解度相等时的温度范围是20℃-30℃℃.
(3)用50g蒸馏水配制40℃时KCl的饱和溶液,需KCl固体质量是20g,操作步骤是:计算、称量溶解.
(4)将40℃时KCl的饱和溶液与KNO3的饱和溶液个100g降温至10℃,对所得溶液的描述正确的是AC(填序号)
A.都是饱和溶液 B.溶液质量:KCl<KNO3 C.溶剂重量:KCl>KNO3.
13.下列气体能直接用湿润的石蕊试纸检验的气体是( )
| A. | CO | B. | CH4 | C. | CO2 | D. | O2 |
14.如图为某化工企业生产流程示意图,有关说法正确的是( )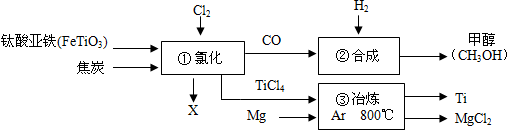

| A. | ③中氩气(Ar)作保护气 | |
| B. | 钛酸亚铁(FeTiO3)中钛元素为+3价 | |
| C. | ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7:1 | |
| D. | ①中反应为2FeTiO3+6C+7Cl2$\frac{\underline{\;一定条件\;}}{\;}$2x+2TiCl4+6CO,则x为FeCl2 |