题目内容
19.某同学称取10克石灰石放入试管中,然后加入20克盐酸溶液恰好完全反应,制得二氧化碳气体2.2克.已知石灰石中的杂质不参加反应,列式计算:(1)石灰石中参加反应的碳酸钙的质量;
(2)该石灰石的纯度(即石灰石中碳酸钙的质量分数);
(3)盐酸溶液的浓度(即盐酸溶液的溶质质量分数).
分析 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据二氧化碳的质量可以计算碳酸钙的质量和氯化氢的质量,进一步可以计算该石灰石样品中碳酸钙的质量分数和所用稀盐酸的溶质质量分数.
解答 解:设碳酸钙的质量为x,20g稀盐酸中氯化氢的质量为y,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 44
x y 2.2g
$\frac{100}{x}=\frac{73}{y}=\frac{44}{2.2g}$
x=5g,y=3.65g,
该石灰石样品中碳酸钙的质量分数为:$\frac{5g}{10g}$×100%=50%,
所用稀盐酸的溶质质量分数为:$\frac{3.65g}{20g}$×100%=18.25%.
答:
(1)石灰石中参加反应的碳酸钙的质量为5g;
(2)该石灰石样品中碳酸钙的质量分数为50%.
(3)所用稀盐酸的溶质质量分数为18.25%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
9.在由A,B两种元素组成的某化合物中,A,与B的质量比为21:8,又知A与B的相对原子质量为7:2,则A,B元素组成的化合物的化学式为( )
| A. | A4B3 | B. | A3B2 | C. | A3B4 | D. | A2B3 |
7.如图是溶解度曲线图,下列说法正确的是( )
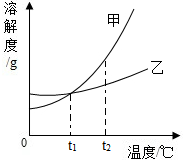

| A. | 甲乙两种溶解度在t1时相等 | |
| B. | 从含有少量乙的溶液中将乙分离出来,应用降低温度 | |
| C. | 从t2降温到t1时,乙析出的固体比甲多 | |
| D. | 甲可能是氯化钠 |
14.下列符号既能表示一种元素,又能表示一种原子,还能表示这种物质的化学式的是( )
| A. | N2 | B. | H2O | C. | Cu | D. | Cl |
11.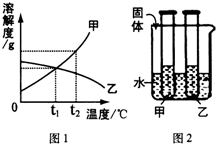 如图1是甲、乙两种固体物质的溶解曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中正确的是( )
如图1是甲、乙两种固体物质的溶解曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中正确的是( )
 如图1是甲、乙两种固体物质的溶解曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中正确的是( )
如图1是甲、乙两种固体物质的溶解曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中正确的是( )| A. | t2℃时,配制等质量的甲、乙两种物质的饱和溶液,甲需要水多 | |
| B. | 将甲、乙两种物质的饱和溶液都从t2℃降至t1℃时,两种溶液中溶质的质量分数相等 | |
| C. | 向烧杯的水中加NaOH固体后,乙溶液中溶质的质量分数变小 | |
| D. | 向烧杯的水加NH4NO3固体后,盛放甲、乙两溶液的试管都中有晶体析出 |