题目内容
15.从金银花中提取的绿原酸(其化学式为C16H18O9)有很高的药用价值.下列有关绿原酸的说法正确的是( )| A. | 绿原酸属于混合物 | |
| B. | 绿原酸相对分子质量为354 | |
| C. | 组成绿原酸的三种元素中氧元素的质量分数最高 | |
| D. | 绿原酸中碳、氢元素的质量比为16:18 |
分析 A.根据物质的分类来分析;
B.根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断;
C.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断;
D.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
解答 解:A、绿原酸是由一种物质组成的,属于纯净物,故选项说法错误.
B、绿原酸的相对分子质量为12×16+1×18+16×9=354,故选项说法正确.
C、绿原酸中碳、氢、氧三种元素的质量比为(12×16):(1×18):(16×9)=96:9:72,因此绿原酸中碳元素的质量分数最高,故选项说法错误.
D、绿原酸中碳、氢元素的质量比为(12×16):(1×18)≠16:18,故选项说法错误.
故选:B.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
3. 根据某物质在不同质量的水中达到饱和状态时所溶解物质的质量,绘制成如图中斜线.下列说法不正确是( )
根据某物质在不同质量的水中达到饱和状态时所溶解物质的质量,绘制成如图中斜线.下列说法不正确是( )
 根据某物质在不同质量的水中达到饱和状态时所溶解物质的质量,绘制成如图中斜线.下列说法不正确是( )
根据某物质在不同质量的水中达到饱和状态时所溶解物质的质量,绘制成如图中斜线.下列说法不正确是( )| A. | 该物质的溶解度随温度的升高而增大 | |
| B. | 某温度时该物质的溶解度为40g | |
| C. | m点表示溶液中溶质的质量分数为20% | |
| D. | 图中4个点表示的溶液中溶质质量分数的关系是:G<m<w=z |
10.仔细观察下列图象,得到结论正确的( )
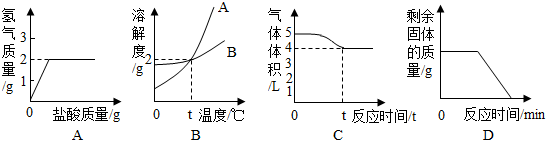

| A. | 图1:在100gCu-Zn合金中加入足量的稀盐酸,根据氢气质量可知合金中Cu的质量分数为35% | |
| B. | 图2:t℃时两种物质的溶解度相同,在t℃时两种溶液溶质质量分数也相同 | |
| C. | 图3:将一定体积的空气通过灼热的铜网充分反应,可知氧气的质量约占空气质量的$\frac{1}{5}$ | |
| D. | 图4:用一定量的木炭还原氧化铜,剩余固体质量与反应时间的关系 |
20.下列化肥中,不加任何试剂即可与其他化肥相区别的是( )
| A. | 硫酸钾 | B. | 碳酸氢铵 | C. | 硝酸铵 | D. | 氯化铵 |
4.一瓶未贴标签的粉末状常见金属R.为了测定R的相对原子质量,准确称取一定量该金属粉末,在坩埚内加强热使其完全氧化,冷却后再称重.重复实验,获得如表数据.请回答:
(1)表格中m=85.0.
(2)已知R的化合价为+3价,则R的相对原子质量为27.
(3)若用该金属与稀硫酸反应制取10L氢气来制气球(H2 密度:0.09克/升),理论上至少需要R多少克?
| 实验次数 | 金属质量(g) | 金属氧化物质量(g) |
| l | 45.0 | 84.9 |
| 2 | 45.0 | 85.1 |
| 3 | 45.0 | 85.O |
| 平均值 | 45.0 | m |
(2)已知R的化合价为+3价,则R的相对原子质量为27.
(3)若用该金属与稀硫酸反应制取10L氢气来制气球(H2 密度:0.09克/升),理论上至少需要R多少克?
 生活中处处有化学.铁锅是厨房中常用的炊具,请用所学的化学知识真空.
生活中处处有化学.铁锅是厨房中常用的炊具,请用所学的化学知识真空.