题目内容
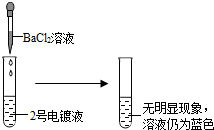
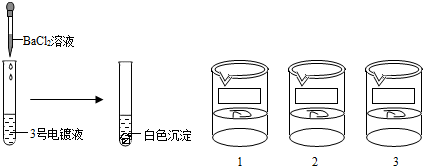
电镀是金属防锈的方法之一.某兴趣小组同学用标为A、B、C的三只试剂瓶,从电镀厂取来ZnSO4、CuSO4和AgNO3三种电镀液.由于忘记每瓶中装的是何种溶液,所以分别取出三种电镀液进行了探究.

根据以上实验回答:
(1)写出电镀液的名称:A瓶中________ B瓶中________
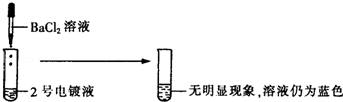
(2)如果实验Ⅱ中将硝酸钡溶液替换为氯化钡溶液,对实验结果________(填“有”或“无”)影响.
(3)小敏同学提出只需选择一种金属单质放入上述三种电镀液中的两种,就可探究出三种电镀液中所含金属的活动性,得到大家一致认可.该金属________.
(4)小冬同学通过查阅资料可知,AgNO3需避光保存,否则会分解生成单质银、NO2和一种助燃的气体.该物质见光发生分解反应的方程式为________
(5)写出A与氢氧化钠溶液反应的化学方程式________.
解:(1)由于硫酸铜溶液显蓝色,所以A瓶中是硫酸铜溶液,B中溶液滴加硝酸钡溶液生成白色沉淀,说明B是硫酸锌溶液,因为硝酸银溶液与硝酸钡不反应;
(2)若实验Ⅱ中将硝酸钡溶液替换为氯化钡溶液,氯化钡也可与硝酸银溶液反应生成氯化银沉淀,故无法判断硝酸银、硫酸锌,对实验结果有影响;
(3)根据金属活动性顺序表可知,三种金属的活动性顺序是:锌、铜、银,所以若探究三种电镀液中所含金属的活动性,可取铜丝与硫酸锌溶液、硝酸银溶液;
(4)依据题意:AgNO3见光会分解生成单质银、NO2和一种助燃的气体氧气,方程式是:2AgNO3 2Ag+2NO2+O2↑;
2Ag+2NO2+O2↑;
(5)硫酸铜与氢氧化钠的反应生成了氢氧化铜沉淀和硫酸钠,反应的方程式是:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.
故答案为:(1)硫酸铜溶液,硫酸锌溶液;(2)有;(3)铜丝;(4)2AgNO3 2Ag+2NO2+O2↑;(5)2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.
2Ag+2NO2+O2↑;(5)2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.
分析:(1)依据硫酸铜溶液显蓝色判断分析A瓶中的溶液,根据硫酸锌可与硝酸钡反应生成硫酸钡沉淀进行判断B瓶中的溶液;
(2)根据氯化钡溶液也可与硫酸锌、硝酸银反应生成不溶于水的沉淀分析解答;
(3)要验证三种金属的活动性,可据“两金夹一盐”或“两盐夹一金”的方法设计实验验证;
(4)根据氧气具有助燃性,硝酸银见光分解的反应原理分析解答;
(5)根据硫酸铜与氢氧化钠的反应写出反应的方程式.
点评:含铜离子的溶液显蓝色,并能据物质的性质、及相互之间的反应分析解答,要根据题目所给信息仔细分析解答.
(2)若实验Ⅱ中将硝酸钡溶液替换为氯化钡溶液,氯化钡也可与硝酸银溶液反应生成氯化银沉淀,故无法判断硝酸银、硫酸锌,对实验结果有影响;
(3)根据金属活动性顺序表可知,三种金属的活动性顺序是:锌、铜、银,所以若探究三种电镀液中所含金属的活动性,可取铜丝与硫酸锌溶液、硝酸银溶液;
(4)依据题意:AgNO3见光会分解生成单质银、NO2和一种助燃的气体氧气,方程式是:2AgNO3
 2Ag+2NO2+O2↑;
2Ag+2NO2+O2↑;(5)硫酸铜与氢氧化钠的反应生成了氢氧化铜沉淀和硫酸钠,反应的方程式是:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.
故答案为:(1)硫酸铜溶液,硫酸锌溶液;(2)有;(3)铜丝;(4)2AgNO3
 2Ag+2NO2+O2↑;(5)2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.
2Ag+2NO2+O2↑;(5)2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.分析:(1)依据硫酸铜溶液显蓝色判断分析A瓶中的溶液,根据硫酸锌可与硝酸钡反应生成硫酸钡沉淀进行判断B瓶中的溶液;
(2)根据氯化钡溶液也可与硫酸锌、硝酸银反应生成不溶于水的沉淀分析解答;
(3)要验证三种金属的活动性,可据“两金夹一盐”或“两盐夹一金”的方法设计实验验证;
(4)根据氧气具有助燃性,硝酸银见光分解的反应原理分析解答;
(5)根据硫酸铜与氢氧化钠的反应写出反应的方程式.
点评:含铜离子的溶液显蓝色,并能据物质的性质、及相互之间的反应分析解答,要根据题目所给信息仔细分析解答.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目