题目内容
有①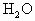 、②HCl、③
、②HCl、③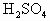 、④
、④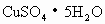 、⑤
、⑤ ⑥NaOH、⑦
⑥NaOH、⑦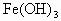 等物质,回答:(填序号)
等物质,回答:(填序号)
(1)属于酸性氧化物的是________;(2)能形成酸式盐的酸是________;
(3)属于盐类的是________;(4)属于难溶性碱的是________.
答案:
解析:
解析:
|
(1)⑤;(2)③;(3)④;(4)⑦ |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
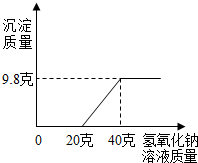 有一定量含HCl、CuSO4的溶液,往其中滴入溶质质量分数为40%的氢氧化钠溶液,反应生成的沉淀如图所示.则溶液中溶质HCl的质量是( )
有一定量含HCl、CuSO4的溶液,往其中滴入溶质质量分数为40%的氢氧化钠溶液,反应生成的沉淀如图所示.则溶液中溶质HCl的质量是( )| A、20克 | B、40克 | C、9.8克 | D、7.3 |
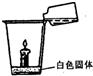 24、小明家中有小小实验室,他收集的物质有①溶液:HCl、AgNO3、Ba(OH)2和H2SO4;②固体:NaCl、CaCO3、CuO和Na2CO3.小明按如图所示的方法实验,有气泡产生,一会儿蜡烛熄灭,白色固体消失.看到上述现象后,小明的同学小亮认为试剂瓶中的溶液为盐酸,玻璃杯中的固体为碳酸钙.除此之外,你认为溶液和固体的组合还可能是什么?请填入表中(任写三种不同组合).
24、小明家中有小小实验室,他收集的物质有①溶液:HCl、AgNO3、Ba(OH)2和H2SO4;②固体:NaCl、CaCO3、CuO和Na2CO3.小明按如图所示的方法实验,有气泡产生,一会儿蜡烛熄灭,白色固体消失.看到上述现象后,小明的同学小亮认为试剂瓶中的溶液为盐酸,玻璃杯中的固体为碳酸钙.除此之外,你认为溶液和固体的组合还可能是什么?请填入表中(任写三种不同组合).