题目内容
12.人类在生产和生活中广泛使用金属.请运用化学知识回答以下问题:(1)下列实验用品中,属于金属材料的是b.(填序号)
a.试管 b.铁架台 c.蒸发皿
(2)下列物质中,不属于合金的是b.(填序号)
a.黄铜 b.氧化汞 c.生铁
(3)下列有关合金的说法错误的是c.(填序号)
a.属于混合物 b.一定含金属元素 c.硬度比其组分金属低
(4)为了防止自行车的链条生锈,常采用的方法是涂油.
(5)用铁锅炒菜主要是利用铁具有良好的导热性,同时还可补充人体所需的铁元素,如果铁元素摄入量过少会引起贫血.
(6)将铁粉投入AgNO3的溶液中,充分反应后过滤,若向滤渣中滴加稀盐酸,有气泡冒出.则滤液中含有的溶质是Fe(NO3)2(写化学式).
分析 (1)金属材料包括纯金属和合金,据此结合常见物质的组成进行分析判断即可.
(2)从合金定义和特征来判断
(3)从合金定义和特征来判断.
(4)根据铁生锈的条件分析;
(5)炒菜时,燃气灶的火焰呈黄色,锅底出现黑色物质,是由于燃气燃烧不充分造成的以及灭火原理进行分析解答;
(6)根据金属的活动性顺序来分析解答.
解答 解:(1)试管是玻璃制成的,蒸发皿是陶瓷制成的,陶瓷、玻璃属于无机非金属材料;铁架台是由生铁制成的,生铁属于金属材料;故填:b;
(2)合金是指一种或几种金属或非金属融合到另一金属中形成的具有金属特性的混合物,而氧化汞是由汞和氧组成的化合物,而不是混合物,故填:b;
(3)合金是指一种或几种金属或非金属融合到另一金属中形成的具有金属特性的混合物,合金与其组成金属相比,熔点降低、硬度增大,故填:c;
(4)铁生锈的条件是与空气中的氧气和水接触,所以防止自行车链条生锈的常用措施是涂油等.故答案为:涂油;
(5)用铁锅炒菜主要是利用铁具有良好的导热性,人体缺铁易患贫血.故填:导热;贫血;
(6)将铁粉投入AgNO3的溶液中,充分反应后过滤,若向滤渣中滴加稀盐酸,有气泡冒出,说明铁粉有剩余,则硝酸银中的银已被完全置换出来;铁与硝酸银反应生成银和硝酸亚铁;故填:Fe(NO3)2
点评 本题难度不大,只有同学们了解材料的分类、合金的概念与性质、铁的锈蚀条件、金属的性质、金属活动性顺序,就可做好此题.

练习册系列答案
相关题目
3.茶叶中含有的茶氨酸(C7H14O3N2)可以降低血压、提高记忆力、保护神经细胞等.下列有关茶氨酸的说法中,正确的是( )
| A. | 茶氨酸属于有机高分子化合物 | |
| B. | 茶氨酸中碳元素与氢元素的质量比为1:2 | |
| C. | 茶氨酸中碳元素的质量分数最大 | |
| D. | 一个茶氨酸分子中含有一个氮分子 |
20.下面是家庭中常见物质的pH,其中显酸性最强是( )
| A. | 酱油(pH=5) | B. | 厕所清洁剂(pH=1) | C. | 柠檬(pH=3) | D. | 橘子(pH=4) |
4.下列有关实验现象的描述,正确的是( )
| A. | 电解水实验中,与电源负极相连的电极上产生的气体是氢气 | |
| B. | 细铁丝在氧气中燃烧,火星四射,生成红色固体 | |
| C. | 硫在氧气中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体 | |
| D. | 红磷在空气中燃烧产生大量白雾 |
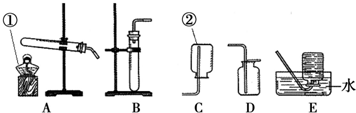
2.实验室常用下列装置来制取、收集气体.仪器b是分液漏斗,可通过旋转活塞分次滴加液体.请回答以下问题.

(1)仪器a、c的名称是:a长颈漏斗,c水槽.
(2)实验室用KMnO4制取02,应选用的发生装置和收集装置的组合为AF或AH(填字母序号),该发生装置的不足之处是试管口没有棉花团,该反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.收集装置的选择是由气体的性质决定的.既能用排水法也能用排空气法收集的气体一定具有的性质有②③(填数字序号)
①易溶于水 ②难溶于水 ③不与水反应
④密度与空气接近 ⑤可与空气中某成分反应 ⑥有毒,是一种大气污染物
(3)实验室要制取少量C02应选择的较简单的发生装置是E(填字母序号).
某同学取一定浓度盐酸与石灰石反应,将生成的气体通入澄清石灰水中,始终未见浑浊,请将可能的原因填入下表(答出两条即可),并就$\underset{其}{•}\underset{中}{•}\underset{一}{•}\underset{条}{•}$$\underset{原}{•}\underset{因}{•}$用简单的实验进行验证:
(4)化学反应可控制才能更好地为人类造福,我们可以通过改变反应的条件、药品用量、改进装置等途径来达到控制反应的目的.常温下块状电石(CaC2)与水反应生成乙炔 (C2H2)气体和氢氧化钙,该反应的化学方程式是CaC2+2H2O=C2H2↑+Ca(OH)2,实验室制取乙炔时,须严格控制加水速度,以免剧烈反应放热引起装置炸裂.图中适合制取乙炔气体的发生装置有D(填装置序号).
(5)某可燃性气体可能是乙炔、甲烷、一氧化碳中的一种或两种.已知13g该气体在足量的氧气中充分燃烧生成44g二氧化碳和9g水,则该气体可能的组成为A.
A.乙炔 B.乙炔和一氧化碳的混合物
C.甲烷和一氧化碳的混合物 D.甲烷和乙炔的混合物.

(1)仪器a、c的名称是:a长颈漏斗,c水槽.
(2)实验室用KMnO4制取02,应选用的发生装置和收集装置的组合为AF或AH(填字母序号),该发生装置的不足之处是试管口没有棉花团,该反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.收集装置的选择是由气体的性质决定的.既能用排水法也能用排空气法收集的气体一定具有的性质有②③(填数字序号)
①易溶于水 ②难溶于水 ③不与水反应
④密度与空气接近 ⑤可与空气中某成分反应 ⑥有毒,是一种大气污染物
(3)实验室要制取少量C02应选择的较简单的发生装置是E(填字母序号).
某同学取一定浓度盐酸与石灰石反应,将生成的气体通入澄清石灰水中,始终未见浑浊,请将可能的原因填入下表(答出两条即可),并就$\underset{其}{•}\underset{中}{•}\underset{一}{•}\underset{条}{•}$$\underset{原}{•}\underset{因}{•}$用简单的实验进行验证:
| 可能的原因 | 实验步骤 | 实验现象 | 实验结论 |
| 原因一: | 猜想的结论正确 | ||
| 原因二: |
(5)某可燃性气体可能是乙炔、甲烷、一氧化碳中的一种或两种.已知13g该气体在足量的氧气中充分燃烧生成44g二氧化碳和9g水,则该气体可能的组成为A.
A.乙炔 B.乙炔和一氧化碳的混合物
C.甲烷和一氧化碳的混合物 D.甲烷和乙炔的混合物.
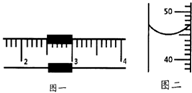 实验室需配制一定溶质质量分数的氯化钠溶液.
实验室需配制一定溶质质量分数的氯化钠溶液.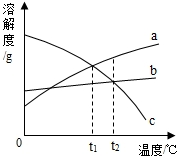 如图是a,b,c三种固体物质的溶解度曲线.据图回答:
如图是a,b,c三种固体物质的溶解度曲线.据图回答: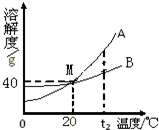 如图分别表示A、B两种物质的溶解度曲线,试回答:
如图分别表示A、B两种物质的溶解度曲线,试回答: