题目内容
10.6.0克含杂质的铁(杂质不溶于水,也不参与反应)与100克CuSO4溶液恰好完全反应,过滤得到干燥的固体6.8克,则所含铁的质量是( )| A. | 6.0克 | B. | 5.6克 | C. | 16克 | D. | 6.4克 |
分析 根据铁和硫酸铜反应生成硫酸亚铁和铜,然后结合题中所给的数据进行解答.
解答 解:设样品中铁的质量为x,
Fe+CuSO4=FeSO4+Cu 固体增加的质量
56 160 64 64-56=8
x y 6.8g-6g=0.8g
$\frac{56}{x}$=$\frac{8}{0.8g}$
x=5.6g
故选:B.
点评 掌握化学方程式的计算格式和规范性,本题的难点是分析固体的成分的计算,一定要考虑杂质的质量.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
5.向下列物质中分别加入足量的蒸馏水,搅拌后能形成无色溶液的是( )
| A. | 面粉 | B. | 氯化亚铁 | C. | 食盐 | D. | 食用油 |
6.在“宏观-微观-符号”之间建立联系,是化学学科特有的思维方式.如图是某化学反应的微观示意图,从中获取的相关信息正确的是( )
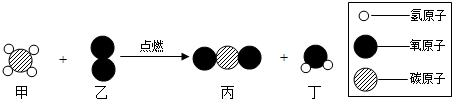

| A. | 甲物质的化学式是CH2 | B. | 丙物质属于氧化物 | ||
| C. | 该反应中有4种化合物 | D. | 甲、乙两物质的质量比为1:1 |
15.下列与燃料或燃烧有关的说法正确的是( )
| A. | 露置在空气中的汽油没有燃烧,因为汽油是液态 | |
| B. | 供家用煤炉燃烧的煤,制成蜂窝状的主要目的是延缓煤的燃烧时间 | |
| C. | 汽油着火应用二氧化碳灭火器,主要目的是隔离空气 | |
| D. | 太阳能热水器的主要工作原理是:水在阳光的照射下发生化学反应 |
2.小根妈妈设计了一份午餐食谱:米饭、清炖牛肉、麻辣豆腐.小明觉得这份食谱营养不够全面,应加上下列中的( )后才能使之合理.
| A. | 素炒豆角 | B. | 牛奶 | C. | 鸡蛋 | D. | 小米粥 |
19.等质量的碳和一氧化碳分别与足量的氧气反应,下列说法中正确的是( )
| A. | 碳需要的氧气多 | B. | 一氧化碳需要的氧气多 | ||
| C. | 生成的二氧化碳一样多 | D. | 一氧化碳生成的二氧化碳多 |
20.碳元素是组成许多物质的基本元素.

(1)甲烷是一种清洁能源,请写出甲烷完全燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)分析下表,与煤相比,用天然气作燃料的优点有等质量的天然气与煤相比,燃烧时热值更高、产生的二氧化碳更少.
(3)为提高煤的利用率,可将其转化为可燃性气体,该反应的微观示意图如下,则生成物的分子个数比为1:1.
(4)化石燃料主要包括煤、石油和天然气.
(5)液态二氧化碳可用于扑救档案室发生的火灾,下列说法正确的是AB(填字母序号).
A.液态二氧化碳汽化后不会污染档案
B.二氧化碳可覆盖在可燃物表面,隔绝空气
C.液态二氧化碳汽化时吸热,降低可燃物的着火点.

(1)甲烷是一种清洁能源,请写出甲烷完全燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)分析下表,与煤相比,用天然气作燃料的优点有等质量的天然气与煤相比,燃烧时热值更高、产生的二氧化碳更少.
| 1g物质完全燃烧 | ||
| 产生二氧化碳的质量/g | 放出的热量/kJ | |
| 甲烷 | 2.75 | 56 |
| 碳 | 3.67 | 32 |
(4)化石燃料主要包括煤、石油和天然气.
(5)液态二氧化碳可用于扑救档案室发生的火灾,下列说法正确的是AB(填字母序号).
A.液态二氧化碳汽化后不会污染档案
B.二氧化碳可覆盖在可燃物表面,隔绝空气
C.液态二氧化碳汽化时吸热,降低可燃物的着火点.