题目内容
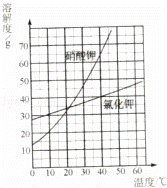
如图是氯化钾和硝酸钾两种固体溶解度曲线图.
(1)20℃时,KNO3的溶解度是 (填“大于”、“小于”或“等于”)KCl的溶解度.
(2)40℃时,KCl的溶解度是 g,向100g水中加入40gKCl,所得溶液中溶质与溶液的质量比为 .
(3)比较这两种物质溶解度曲线的变化规律,从中你可以获得哪些信息: (任写一条).
(4)下列说法正确的是 .
A.KNO3饱和溶液一定比不饱和溶液浓
B.饱和KCl溶液析出晶体后,溶液中溶质的质量分数可能不变
C.30℃时,分别将10g KCl和10g KNO3配制成饱和溶液,前者需要水的质量较多
D.分别将40℃时的KCl和KNO3的饱和溶液降温到20℃时,后者析出的晶体较多.
| 固体溶解度曲线及其作用;饱和溶液和不饱和溶液;晶体和结晶的概念与现象. | |
| 专题: | 溶液、浊液与溶解度. |
| 分析: | (1)根据溶解度曲线图解答; (2)根据溶解度曲线表查出氯化钾的溶解度;根据氯化钾的溶解度曲线可知,40℃时氯化钾的溶解度为40g进行解答; (3)根据溶解度曲线表示的意义,交点的含义,溶解度大小的比较方法考虑本题; (4) A、根据温度不同解答; B、根据在同一温度下的饱和溶液中溶质的质量分数可能不变解答; C、根据硝酸钾和氯化钾的溶解度受温度影响情况解答; D、根据不知硝酸钾和氯化钾的饱和溶液的质量关系解答. |
| 解答: | 解: (1)由溶解度曲线图可知20℃时,KNO3的溶解度是小于KCl的溶解度; (2)由溶解度曲线可知40℃时,氯化钾的溶解度为40g;即在40℃100g水中溶解40g氯化钾达到饱和,所以40℃时,向100g水中加入40gKCl,所得溶液中溶质与溶液的质量比为40g:140g=2:7; (3)曲线越陡受温度影响就大,所以硝酸钾的溶解度受温度的影响大,氯化钾物质受温度影响较小; (4) A、不知温度,无法比较饱和溶液与不饱和溶液的浓稀,故错; B、在同一温度下,饱和KCl溶液析出晶体后,溶液中溶质的质量分数可能不变,故对; C、30℃时,KCl的溶解度小于 KNO3的溶解度,分别将10g KCl和10g KNO3配制成饱和溶液,前者需要水的质量较多,故对; D、知硝酸钾和氯化钾的饱和溶液的质量关系,无法比较析出的晶体的多少,故错. 答案: (1)小于 (2)40 2:7 (3)硝酸钾的溶解度受温度的影响大,氯化钾物质受温度影响较小 (4)BC |
| 点评: | 本题考查了学生据图表作溶解度曲线及对溶解度曲线意义的了解和应用,能较好考查学生应用知识解决问题的能力. |

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案铈(Ce)是一种常见的稀土元素,下列有关说法中不正确的是( )

|
| A. | 铈的相对原子质量是140.1g | B. | 铈属于金属元素 |
|
| C. | 铈的原子序数是58 | D. | 铈原子核内有58个质子 |
下列有关水的说法错误的是( )
|
| A. | 水是氧化物 |
|
| B. | 煮沸可降低自来水的硬度 |
|
| C. | 肥皂水可区分硬水和软水 |
|
| D. | 电解水的实验,说明水是由氢气和氧气组成的 |
下列有关二氧化碳的说法正确的是( )
|
| A. | 实验室常用块状石灰石和稀硫酸反应制取二氧化碳气体 |
|
| B. | 二氧化碳用于人工灭火,既利用了它的物理性质也利用了它的化学性质 |
|
| C. | 二氧化碳可使紫色石蕊试液变蓝将二氧化碳气体通入紫色石蕊试液中,溶液呈红色,说明二氧化碳显酸性 |
|
| D. | 二氧化碳有毒不能制作碳酸饮料将燃着的木条伸入一瓶气体中,木条立即熄灭,证明瓶内原有气体就是二氧化碳 |
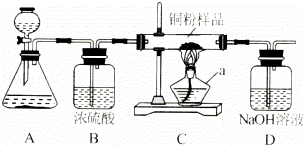
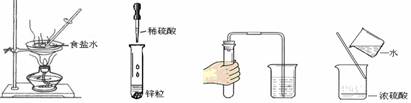
如图所示,某校化学兴趣小组用过氧化氢(H2O2)溶液(MnO2作催化剂)制取干燥的氧气,并用来侧定,1Og某铜粉样品(含杂质碳)中铜的质量分数.回答下列问题:
(1)仪器a的名称是 .
(2)装置A中发生反应的化学方程式是 .装置B的作用是 .
(3)通过称量反应前后装置 的质量,进行计算便可求出样品中铜的质量分数.
(4)实验完毕.小丽同学误将用剩的H202溶液和装置C玻璃管中的剩余固体一起倒入烧杯中,发现有大最的气泡产生,经检验确认产生的气体是氧气.小刚和小明两位同学对此颇感兴趣.进而展开了他们的探究之旅.
【提出问题】是哪种物质加快了H202的分解速率?
【大胆猜想】猜想Ⅰ:剩余固体中的氧化铜加快了H202溶液的分解.
猜想Ⅱ:剩余固体中的 加快了H2O2溶液的分解.
猜想Ⅲ:氧化铜能做H202分解的催化剂.
【实验验证】
| 实验方案 | 实验现象 | 分析及结论 |
| 实验一:将带火星的木条伸入盛有5mL 5%H2O2溶液的试管. | 带火星木条不复燃 | H202溶液常温下产生氧气的量很少,不足以使带火星的木条复燃 |
| 实验二:向盛有5mL5%H202溶液的试管中加入1g氧化铜固体,将一根带火星的木条伸入试管.观察现象.待反应结束后将试管里的剩余物进行 、洗涤、干燥、称量.对比反应前后氧化铜的质量 |
称得固体质量为1g. | 猜想Ⅰ成立.反应前后氧化铜的质量相等. |
| 实验三:向盛有5mL5%H202溶液的试管中加入1g ,将一根带火星的木条伸入试管,观察现象. | 没有气泡产生,带火星 木条不复燃. | 猜想Ⅱ (填”成立“或“不成立”) |
【讨论交流】小刚同学认为,根据实验二得出的两个结论就能判断Ⅲ成立,你是否支持他的观点?并简述理由.
答: . .
 .天然气是较为清洁的可再生能源 D.空气中氧气的体积分数约为78%
.天然气是较为清洁的可再生能源 D.空气中氧气的体积分数约为78%