题目内容
2.粗盐中含有MgCl2、CaCl2等杂质,工业提纯粗盐的工艺流程如下图所示: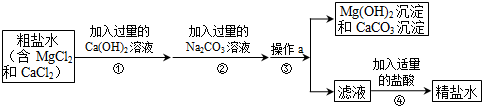
(1)步骤①反应的化学方程式为Ca(OH)2+MgCl2═Mg(OH)2↓+CaCl2.
(2)步骤③操作a的名称是,该操作中玻璃棒的作用是引流
(3)滤液中加稀盐酸发生中和反应方程式NaOH+HCl═NaCl+H2O.
(4)若步骤①和步骤②的顺序颠倒,则最后所得的精盐水中还含有CaCl2.
分析 (1)根据氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙进行分析;
(2)根据过滤可以将固体和液体分离,以及玻璃棒的作用进行分析;
(3)根据盐酸和氢氧化钠反应生成氯化钠和水进行分析;
(4)根据Ca(OH)2可除去MgCl2,Na2CO3可除去CaCl2分析.
解答 解:(1)氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙,化学方程式为:Ca(OH)2+MgCl2═Mg(OH)2↓+CaCl2;
(2)过滤可以将固体和液体分离,所以步骤③操作a的名称是过滤,该操作中玻璃棒的作用是引流;
(3)盐酸和氢氧化钠反应生成氯化钠和水,化学方程式为:NaOH+HCl═NaCl+H2O;
(4)根据Ca(OH)2可除去MgCl2,Na2CO3可除去CaCl2和过量的氢氧化钙,如果步骤①和步骤②的顺序颠倒,步骤②先反应溶液中就有过量的碳酸钠,然后完成步骤①,这时过量的氢氧化钙把上步中多余的碳酸钠除去,同时生成氢氧化钠,另外氢氧化钙与氯化镁反应还生成氯化钙,最后步骤④中加入适量的盐酸,反应掉生成的氢氧化钠,但不与生成的氯化钙反应,所以最后所得的精盐水中还含有CaCl2.
故答案为:(1)Ca(OH)2+MgCl2═Mg(OH)2↓+CaCl2;
(2)过滤,引流;
(3)NaOH+HCl═NaCl+H2O;
(4)CaCl2.
点评 粗盐提纯是经常考查的内容,其中要涉及到化学方程式的书写、过滤操作、杂质的除去等内容,需要同学们对此内容了然于心.

练习册系列答案
相关题目
12.下列物质中,属于纯净物的是( )
| A. | 矿泉水 | B. | 五氧化二磷 | C. | 苹果醋 | D. | 纯牛奶 |
13.(1)在下表的空白处填上恰当的内容:
(2)小丽同学做完镁条在空气中燃烧的实验之后,对该变化的实质进行研究,氧原子和镁原子的结构示意图如图1所示,从氧原子和镁原子的结构示意图可以看出,氧原子和镁原子结合时,氧原子易得到2个电子,镁原子易失去2个电子,形成的两种粒子的符号分别是O2-、Mg2+.
②镁条在空气中燃烧的化学方程式为2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(3)如图2是两种物质发生中和反应的微观示意图,请回答下列问题:
①图中发生中和反应的化学方程式为:HCl+NaOH=NaCl+H2O.
②当恰好完全中和后,反应的实质可以用一个式子表示为H++OH-=H2O,此时溶液中存在的离子是Na+、Cl-(填符号).

| 物质名称 | 物质的组成(用化学式表示) | 构成物质的微粒(用符号表示) |
| 干冰 | ||
| 锌 | ||
| 食盐水 | ---------- |
②镁条在空气中燃烧的化学方程式为2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(3)如图2是两种物质发生中和反应的微观示意图,请回答下列问题:
①图中发生中和反应的化学方程式为:HCl+NaOH=NaCl+H2O.
②当恰好完全中和后,反应的实质可以用一个式子表示为H++OH-=H2O,此时溶液中存在的离子是Na+、Cl-(填符号).

11.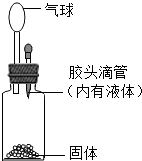 要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
①锌和稀硫酸 ②石灰石和盐酸 ③生石灰和水 ④铁锈和盐酸 ⑤二氧化锰和双氧水 ⑥氢氧化钙和水.
 要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )①锌和稀硫酸 ②石灰石和盐酸 ③生石灰和水 ④铁锈和盐酸 ⑤二氧化锰和双氧水 ⑥氢氧化钙和水.
| A. | ①②③⑤ | B. | ①②④⑤ | C. | ①②④⑤⑥ | D. | ①②③④⑤⑥ |
