题目内容
16.某同学将光亮的镁条放入底油酚酞溶液的NaHCO3饱和溶液中,产生大量气泡和白色固体,溶液红色加深a.溶液红色加深,则反应后溶液的碱性增强(填“增强”、“不变”或“减弱”).
b.为确定该气体和固体的成分,该同学点燃产生的气体,发现火焰呈淡蓝色;将燃烧产物通入澄清石灰水中,无明显现象.则该气体为H2(写化学式).
该同学对白色固体做出如下猜测并进行实验:
【作出猜测】
查阅资料a:Mg(HCO3)2能溶于水.
①白色固体可能是MgCO3;
②白色固体可能是Mg(OH)2;
③白色固体可能是MgCO3和Mg(OH)2.
【设计并进行实验】
(1)取洗净后的白色固体,加入足量的稀盐酸,观察到有气泡产生,则白色固体一定含有MgCO3.
查阅资料b:MgCO3、Mg(OH)2加热易分解,分别生成两种氧化物.
②为进一步确定白色固体的组成,该同学称取适量干燥的白色固体,充分加热至不再产生气体为止,并使分解产生的气体全部先通过浓硫酸,再通过碱石灰,发现浓硫酸和碱石灰都明显增重了,则白色固体中的成分为Mg(OH)2,MgCO3(填化学式)
分析 a.显碱性的溶液能使酚酞试液变红色;
(二)氢气燃烧能够产生淡蓝色火焰,不能与氢氧化钙反应;
【作出猜测】根据质量守恒定律可以判断物质的组成情况;
【设计并进行实验】
碳酸镁能和稀盐酸反应生成氯化镁、水和二氧化碳;
通过计算可以判断物质的质量比.
解答 解:a.溶液红色加深,则反应后溶液的碱性增强.
故填:增强.
b.(1)点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象.则该气体为氢气,氢气的化学式是H2.
故填:H2.
【作出猜测】②白色固体可能是MgCO3,白色固体可能是Mg(OH)2,白色固体可能是MgCO3和Mg(OH)2.
故填:Mg(OH)2.
【设计并进行实验】
(1)取洗净后的白色固体,加入足量的稀盐酸溶液,观察到有气泡产生,则白色固体一定含有MgCO3.
故填:稀盐酸;有气泡产生.
(2)碳酸镁受热分解生成氧化镁和二氧化碳,氢氧化镁受热分解生成氧化镁和水,分解产生的气体全部先通过浓硫酸,浓硫酸增重,说明白色固体中含有氢氧化镁,再通过碱石灰,发现碱石灰明显增重了,说明白色固体中含有MgCO3.
答案:
a.增强
b.H2
【作出猜测】②Mg(OH)2.
【设计并进行实验】
(1)稀盐酸 有气泡产生
(2)Mg(OH)2,MgCO3
点评 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力.所以,对化学实验不仅要认真观察,还应掌握观察实验现象的方法.

练习册系列答案
相关题目
4.下列实验操作中,正确的是( )
| A. | 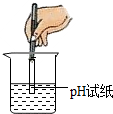 测溶液pH | B. | 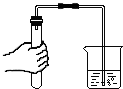 检查装置气密性 | C. | 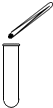 取用固体药品 | D. | 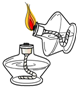 点燃酒精灯 |
1.医务人员用3%的过氧化氢溶液处理外伤口时,伤口上会看到大量的气泡.下列有关说法中正确的是( )
| A. | 生成的气体一定是过氧化氢分解产生的氢气 | |
| B. | 伤口处的生物酶可能对过氧化氢的分解起到催化作用 | |
| C. | 只有二氧化锰能使过氧化氢的分解速率加快 | |
| D. | 过氧化氢和水的分子构成不同,所以它们的性质完全不同 |
18.氧化铟(In2O3)是制作触摸屏的材料之一.氧化铟元素(In)的化合价为( )
| A. | -3 | B. | +2 | C. | +3 | D. | +6 |

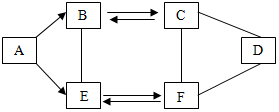 A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示(图中“-”表示反应关系,“→”表示转化关系,部分反应物、生成物及反应条件已略去).已知A、B、C、D、F是不同类别的物质,A、B分别为气体,A是单质,E是相对分子质量最小的氧化物.请回答:
A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示(图中“-”表示反应关系,“→”表示转化关系,部分反应物、生成物及反应条件已略去).已知A、B、C、D、F是不同类别的物质,A、B分别为气体,A是单质,E是相对分子质量最小的氧化物.请回答: