题目内容
1.镍(Ni)是一种重要的金属,能与稀硫酸(或稀盐酸)反应,生成NiSO4(或NiCl2)和氢气,而得到亮绿色溶液.(1)结合已有知识,要得出Ni、Zn、Ag的金属活动性顺序,只要比较Ni、Zn或Ni、Ag的金属活动性顺序即可.某同学利用镍片、锌片和AgNO3溶液,通过实验验证了三种金属活动性顺序为Zn>Ni>Ag,每步反应均充分进行,且均有明显现象.操作如下,将图1中剩余药品填写完整.
(2)某电镀厂废液中含有Ni(NO3)2和AgNO3,为了提取并回收银,设计了下列实验方案(如图2):
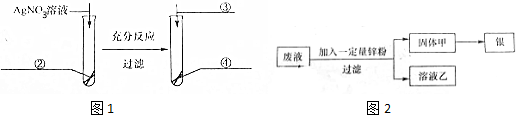
Ⅰ.若溶液乙为亮绿色,则说明固体甲是银.该说法是否正确?说明原因.
Ⅱ.若溶液乙为无色,设计实验验证甲的组成.
Ⅲ.写出由固体甲得到银的实验操作过程.
分析 (1)在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此判断能否发生反应,进而可确定三种金属活动性由强到弱的顺序.
验证三种金属活动性强弱时,通常采取“三取中”的方法,即取中间金属单质与两端的金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应.
(2)排在氢前面的金属,才能置换出酸中的氢;排在金属活动性顺序中前面的金属一般能把排在后面的金属从其盐溶液里置换出来;然后结合实验目的分析实验流程图,并根据对流程图的分析,判断流程中所需加入的物质及发生反应的方程式,设计实验检验反应物是否过量.
解答 解:
(1)结合已有知识,要得出Ni、Zn、Ag的金属活动性顺序,只要比较Ni、Zn或Ni、Ag的金属活动性顺序即可.因为采取“三取中”的方法,即取中间金属单质与两端的金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应,故利用镍片、锌片和AgNO3溶液,通过实验验证了三种金属活动性顺序为Zn>Ni>Ag,结合图,锌与AgNO3溶液反应生成硝酸锌和银,过滤得硝酸锌溶液,硝酸锌溶液与Ni不反应,无现象.图1中②为锌,③为硝酸锌溶液,④为Ni;
(2)在金属活动性顺序中,Zn>Ni>Ag,加入的锌粉能与硝酸银反应生成银,能与Ni(NO3)2反应生成Ni,生成的Ni能与硝酸银反应生成银和硝,故加入的锌粉首先与硝酸银反应,根据流程可知:
Ⅰ.根据含有Ni的溶液为亮绿色,则若溶液乙为亮绿色,则说明固体甲可能是银或Ni、Ag.该说法不正确.
Ⅱ.若溶液乙为无色,说明Ni(NO3)2全反应,则固体甲为Ni、Ag,则滴入硝酸银溶液,如果有灰白色固体生成,而溶液变为亮绿色,则说明有Ni;
Ⅲ.由固体甲得到银的实验操作为:滴入硝酸银溶液,充分反应,过滤.
故答案为:
(1)Ni、Zn或Ni、Ag;②为锌,③为硝酸锌溶液,④为Ni;
(2)Ⅰ.固体甲可能是银或Ni、Ag.该说法不正确.
Ⅱ.滴入硝酸银溶液,如果有灰白色固体生成,而溶液变为亮绿色,则说明有Ni;
Ⅲ.滴入硝酸银溶液,充分反应,过滤.
点评 本题难度不大,考查金属活动性应用,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键.

| 事实 | 解释 | |
| A | 二氧化碳无毒,而一氧化碳有毒 | 物质组成元素不同,分子结构也不同 |
| B | 0℃时水结成冰,而海水在-1.9℃才会结冰 | 海水中溶解的盐,使其凝固点降低 |
| C | 蒸发水和电解水是两种不同类型的变化 | 变化中,前者没有新物质生成,后者有新物质生成 |
| D | KMnO4溶液和K2SO4溶液的颜色不同 | 两种溶液中的阴离子不同 |
| A. | A | B. | B | C. | C | D. | D |
| A. | H2SO4 NaCl Na2CO3 CaCl2 | B. | HCl NaOH CuSO4 MgSO4 | ||
| C. | Na2CO3 K2SO4 BaCl2 HCl | D. | NaNO3 HCl CaCl2 KOH |
| A. | 单质 | B. | 元素 | C. | 分子 | D. | 原子 |


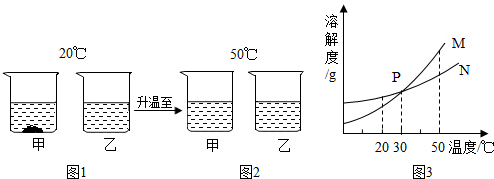




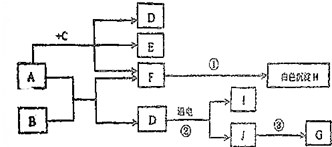 A-J表示初中化学常见的物质,它们之间的转化关系如图所示(部分反应物和生成物已略去).框图中A可用于改良酸性土壤,B是人体胃液中含有的物质,G是红棕色粉末,E、I、G是无色气体.根据图示回答下列问题.
A-J表示初中化学常见的物质,它们之间的转化关系如图所示(部分反应物和生成物已略去).框图中A可用于改良酸性土壤,B是人体胃液中含有的物质,G是红棕色粉末,E、I、G是无色气体.根据图示回答下列问题.