题目内容
一化学兴趣小组对某生铁样品中铁的质量分数进行探究.请按要求完成下列探究报告.
【实验目的】
测定某生铁样品中单质铁的质量分数.
【资料支撑】
生铁中除铁外,还含有碳、硅、锰、磷和硫等元素.碳在生铁中以两种形态存在,一种是游离碳(石墨),另一种是化合碳(如Fe3C等);硅、锰、磷、硫存在形式较为复杂;这些物质通常都不与稀硫酸发生化学反应.
【实验方案】
生铁样品与过量的稀硫酸反应,测定反应前后可称量物质的质量差.
【实验过程】
(1)取一只烧杯,称得其质量为70.4g,加入一定量生铁样品碎屑,称得烧杯和样品的总质量为102.4g;
(2)向盛有生铁样品的烧杯中加入稀硫酸,边加边搅拌,直到烧杯中不再产生气泡,再加入少量稀硫酸以确保过量,测得共用去稀硫酸247.3g;
(3)静置,称量.称得烧杯和剩余物质的总质量为348.7g.
【数据处理】
计算该生铁样品中单质铁的质量分数: .
【交流讨论】
(1)实验称量时称量物应放在托盘天平的 盘(选填“左”或“右”);
(2)实验过程中稀硫酸要过量的原因是 ;
(3)经质检部门精确测定,该样品中铁元素的总含量为95.2%.假设没有与硫酸反应的铁都以Fe3C形式存在,则样品中Fe3C的质量分数为 .
【实验目的】
测定某生铁样品中单质铁的质量分数.
【资料支撑】
生铁中除铁外,还含有碳、硅、锰、磷和硫等元素.碳在生铁中以两种形态存在,一种是游离碳(石墨),另一种是化合碳(如Fe3C等);硅、锰、磷、硫存在形式较为复杂;这些物质通常都不与稀硫酸发生化学反应.
【实验方案】
生铁样品与过量的稀硫酸反应,测定反应前后可称量物质的质量差.
【实验过程】
(1)取一只烧杯,称得其质量为70.4g,加入一定量生铁样品碎屑,称得烧杯和样品的总质量为102.4g;
(2)向盛有生铁样品的烧杯中加入稀硫酸,边加边搅拌,直到烧杯中不再产生气泡,再加入少量稀硫酸以确保过量,测得共用去稀硫酸247.3g;
(3)静置,称量.称得烧杯和剩余物质的总质量为348.7g.
【数据处理】
计算该生铁样品中单质铁的质量分数:
【交流讨论】
(1)实验称量时称量物应放在托盘天平的
(2)实验过程中稀硫酸要过量的原因是
(3)经质检部门精确测定,该样品中铁元素的总含量为95.2%.假设没有与硫酸反应的铁都以Fe3C形式存在,则样品中Fe3C的质量分数为
考点:实验探究物质的组成成分以及含量,称量器-托盘天平,金属的化学性质,酸的化学性质,根据化学反应方程式的计算
专题:科学探究
分析:烧杯中减少的质量是生成氢气的质量,根据铁与稀硫酸反应的化学方程式可以计算出样品中单质铁的质量.进而计算出样品中单质铁的质量分数.
由样品质量和样品中铁元素的质量分数,可以计算出样品中铁元素的总质量,去掉单质铁的质量,就是没有与稀硫酸反应的铁元素的质量,根据物质中某元素的质量分数的计算公式可以计算出样品中Fe3C的质量,进而计算出样品中Fe3C的质量分数.
由样品质量和样品中铁元素的质量分数,可以计算出样品中铁元素的总质量,去掉单质铁的质量,就是没有与稀硫酸反应的铁元素的质量,根据物质中某元素的质量分数的计算公式可以计算出样品中Fe3C的质量,进而计算出样品中Fe3C的质量分数.
解答:解:生成H2的质量:102.4g+247.3g-348.7g=1.0g
设生铁样品中含铁的质量为x.
Fe+H2SO4═FeSO4+H2↑
56 2
x 1.0g
根据:
=
,解得x=28.0g
生铁样品中铁单质的质量分数为
×100%=87.5%
答:生铁样品中铁单质的质量分数是87.5%.
(1)称量时物品放在天平的左盘,砝码放在天平的右盘
(2)实验过程中稀硫酸要过量的原因是确保生铁样品中铁单质与稀硫酸完全反应
(3)设样品质量为100g,则样品中铁元素的总质量为
100g×95.2%=95.2g.铁单质的质量为100g×87.5%=87.5g
样品中Fe3C的铁元素质量为95.2g-87.5g=7.7g
7.7g÷(
×100%)=8.25g
样品中Fe3C的质量分数为
×100%=8.25%
答:生铁样品中单质铁的质量分数为87.5%
故答案为:
87.5%;(1)左;(2)确保生铁样品中铁单质与稀硫酸完全反应;(3)8.25%.
设生铁样品中含铁的质量为x.
Fe+H2SO4═FeSO4+H2↑
56 2
x 1.0g
根据:
| 56 |
| 2 |
| x |
| 1.0g |
生铁样品中铁单质的质量分数为
| 28.0g |
| 102.4g-70.4g |
答:生铁样品中铁单质的质量分数是87.5%.
(1)称量时物品放在天平的左盘,砝码放在天平的右盘
(2)实验过程中稀硫酸要过量的原因是确保生铁样品中铁单质与稀硫酸完全反应
(3)设样品质量为100g,则样品中铁元素的总质量为
100g×95.2%=95.2g.铁单质的质量为100g×87.5%=87.5g
样品中Fe3C的铁元素质量为95.2g-87.5g=7.7g
7.7g÷(
| 56×3 |
| 180 |
样品中Fe3C的质量分数为
| 8.25g |
| 100g |
答:生铁样品中单质铁的质量分数为87.5%
故答案为:
87.5%;(1)左;(2)确保生铁样品中铁单质与稀硫酸完全反应;(3)8.25%.
点评:本题主要考查有关化学方程式的计算和化学式的计算,难度较大.

练习册系列答案
相关题目
元素X的原子的最外层有1个电子,元素Y的原子最外层有6个电子.有X,Y两种元素形成的化合物的化学式可能是( )
| A、XY2 |
| B、X2Y |
| C、XY |
| D、X4Y |
在一定质量的氯酸钾(KClO3)中加入少量的二氧化锰(MnO2)并加热生成氯化钾(KCl)和氧气(O2),到不再产生气体为止,如图不能正确表示反应前后各物质的质量变化(m)与时间(t)关系的是( )
A、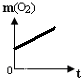 |
B、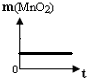 |
C、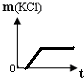 |
D、 |
下列描述不正确的是( )
| A、铁生锈是缓慢氧化 |
| B、吹灭蜡烛是因为降低了蜡烛的着火点 |
| C、酒精燃烧用湿布盖灭 |
| D、扑灭电器、图书档案等火灾最适宜的灭火器是液态二氧化碳灭火器 |
下列甲乙丙丁四位同学对物质性质的描述中,属于化学性质的是( )
| A、甲:“镁条可以在空气中燃烧” |
| B、乙:“水常温下是一生种无色透明的液体” |
| C、丙:“高锰酸钾是暗紫色固体” |
| D、丁:“蜡烛不溶于水,密度比水小” |
以下关于碳和碳的氧化物的说法中,正确的是( )
| A、C、CO和CO2都具有还原性 |
| B、金刚石、石墨、C60都是由碳原子构成的,性质相同 |
| C、用石蕊溶液可区分CO和CO2 |
| D、碳具有可燃性,因此,在常温下其化学性质比较活泼 |

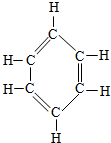 2014年4月10日17时,兰州市威立雅水务集团公司检测显示,出厂水中苯含量严重超标.苯在常温下是一种无色、有芳香气味的透明液体,难溶于水,具有可燃性,结构式如图所示.自来水受到苯污染后,专家建议在水中加入一定量的活性炭,8至10分钟后滤出,可除去水中90%的苯.
2014年4月10日17时,兰州市威立雅水务集团公司检测显示,出厂水中苯含量严重超标.苯在常温下是一种无色、有芳香气味的透明液体,难溶于水,具有可燃性,结构式如图所示.自来水受到苯污染后,专家建议在水中加入一定量的活性炭,8至10分钟后滤出,可除去水中90%的苯.